网址:http://m.1010jiajiao.com/timu_id_127924[举报]
1.A 2.B 3.D 4.A 5.A 6.B 7.B 8.C 9.D 10.C 11.A 12.C
13.(第一空2分,其余空各1分,共6分)
反应物原子间有电子转移 得 降低 还原 还原
14.(空各2分,共6分)②⑦ ①⑧ ④⑤
15.(方程式各3分,共6分)
(1)CaCO3 + 2H+ = Ca2++ 2H2O + CO2↑
(2)Cu2++ SO42- + Ba2++ 2OH-== Cu(OH)2↓+ BaSO4↓
16.(方程式各3分,共6分)
(1)Na2CO3 + 2HC1 = CO2↑+ H2O + 2NaC1
(2)AgNO3+ HC1 = AgC1↓+ HNO3
17.(每小题各2分,共8分) 略。
18.(空各2分,方程式各3分,共14分)
(1)Na2CO3、BaCl2、AgNO3、HCl
(2)CO32- + 2H+ = CO2↑+ H2O ; Ag+ + C1- = AgC1↓
19.(空各3分,共6分) 7.1 7.3
第二章 参考答案
1.B 2.A 3. B 4. C 5. C 6. D 7. C 8. D 9. C 10.B 11.A 12. A
13.银白; Na2O2; 黄; 软;2Na+2H2O=2NaOH+H2↑;(略);Fe3++3OH-=Fe(OH)3↓;
产生红褐色沉淀。
14.风化; 潮解; Na2CO3; 不变。
15.Na+>K+>Rb+; 还原; Rb、K、Na。
16.HCO3-+H+=H2O+CO2↑; 2OH-+CO2=CO32-+H2O; CO32-+H2O+CO2=2HCO3-
17.(1)ac (2)①FeCl3; 2Fe3++Fe=3Fe2+,防止Fe2+被氧化成Fe3+
②产生白色沉淀,迅速变成灰绿色,最终变为红褐色沉淀;4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(3)Al(OH)3, Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+3H+=Al3++3H2O。
第三章 参考答案
16.18.4%
17.
第四章 参考答案
1.D 2.C 3.C 4.C 5.B 6.C 7.C
8.B 9.C 10.D 11.B 12.D 13.D 14.A
15.③④②①; ④③①②; ④③①②; ③②④①; ④③②①;
16.(1) E C D A B H G F
(2)MnO2+4HCl
(浓)  MnCl2+Cl ↑+2H2O
MnCl2+Cl ↑+2H2O
(3)①除去Cl3中的HCl气体 ②除去Cl2中混有的水蒸气
(4)Cl2+2OH-=Cl-+ClO-+H2O
17.(1)
第五章 参考答案
1.C 2.C 3.B 4.B 5.C 6.B 7.B 8.C 9.C 10.B
11.互为同位素 1:2:3 1:1:1 1:1:1
12.Na2O K2S MgF2 CaCl2
13.(1)A:氧 B:磷 C:硫 D:氯 E:铝
(2) A离子: C原子:
C原子:
(3) 极性
(4)先有白色沉淀产生并逐渐增多,随NaOH加入又逐渐溶解最终澄清
Al3++3OH-=Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O
14.(1)A B
(2) ① Cl2+H2O = H+ + Cl‑ + HClO ② 略 ③ 2K2O2+2CO2=2K2CO3+O2
第六章 参考答案
1.B 2.B 3.D 4.D 5.B 6.A 7.B 8.B 9.C 10.D
11.
(1)氧化 (2)还原 (3)
12.(1)①如图配置

②打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加。
(2)①溶液褪色 ②溶液褪色 ③有浅黄色沉淀(或溶液变浑浊)
(3)①NaSO3 变质 取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再
滴入BaCl2 ,溶液有白色沉淀生成,则证明该NaSO3 固体变质
②不是浓硫酸 用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸
13. (1) O2
(1) O2
(2)C + 2H2SO4 (浓) 2SO2 + CO2↑+ 2H2O
(3)CO + 2H+
+ 2H+ CO2↑+
H2O SO2 + Cl2 + 2H2O
4H + + SO + 2Cl ?
+ 2Cl ?
第七章 参考答案
1.D 2.C 3.D 4.B 5.B 6.C 7.D 8.A 9.C 10.C 11.C
12. (1)a、c、d、e? (2)浓HNO3、水、块状大理石
13. (1)B装置中导气管长进短出
(2)①Cu + 2H2SO4(浓) CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O
②反应过程中H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应;
③A、D
14.解:⑴ Cu+2H2SO4(浓) CuSO4
+SO2↑+2H2O ⑵Cu
CuSO4
+SO2↑+2H2O ⑵Cu H2SO4
H2SO4  CuSO4
CuSO4
6
⑶c(CuSO4)======0.2mol?L-1 答:(略)
(11分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验:
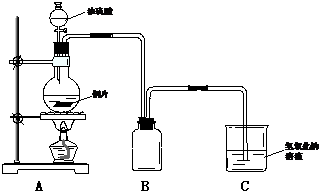
(1)实验中他们取6.4g铜片和12mL 18mol?L![]() 浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜跟浓硫酸反应的化学方程式:______________________________。
②下列药品中能够用来证明反应结束后烧瓶中确有余酸的是 (填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
③为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是: 。
(2)甲学生设计测定余酸的物质的量浓度的实验方案是测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度,他认为测定SO2的量的方法有多种,下列实验方案中不可行的是_____ __(填写字母编号)。
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将产生的气体缓缓通入足量酸性KMnO4溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(标准状况下)
D.用排饱和NaHSO3溶液的方法测出装置A产生气体的体积(标准状况下)
(3)乙学生设计测定余酸的物质的量浓度的实验方案是:测定反应后混合溶液中Cu2+的量。在反应后的溶液中加蒸馏水稀释至100mL,加入足量Na2S溶液,充分反应后过滤,再将沉淀洗涤、干燥、称量。
请写出生成沉淀的离子方程式:
(4)图中C是尾气处理装置,但常常产生倒吸现象,请你设计实验装置,防止倒吸现象的发生,在右图中补充完整: