网址:http://m.1010jiajiao.com/timu_id_126199[举报]
行走的成年礼
李晋
①记得在拉萨布达拉宫的广场上碰到一个朋友,他羡慕我的年轻,说自己如果能早几年来拉萨,他的人生必将是不同的景致。可是现实中的牵绊已经不允许他重新来过,因此他的生活中留下了永远的遗憾。
②我喜欢旅行中坐在长途车上产生的错觉,它赋予我平日里没有的敏感。我相信人们在行走中会变得聪明,因为4年来我几乎所有重要的决定,都是在旅行中做出的,我在不同的文化间寻找着自己,那种浪漫与坚持,有点像少年的游戏。
③日常生活总是单调而枯燥的,在不断的模仿与复制中,人们很容易迷失自己,只有车窗外那不断变幻的风景,还在以一种镜像,映射出我的存在。于是在行走的背后,每个人都不由得变得坚强,我们不断地反思过去,寻找着超越的可能。
④当原本的厌倦与懈怠从身上剥离时,我们在旅行中便实现了对自我的回归。那是一种奇妙的境界,把生命带回到初始时的样子,它是如此清新,一尘不染。我们在行走中还能接触到其他人,接触和吸收异域的新鲜文化,这种文化间的相逢,同样给一个人的生活方向提供无限可能。
⑤旅行赋予我们新生,它为我们描绘出一幅奇异的影像,那里有生命的原初和价值的多元。记得巴西作家保罗·科埃略曾写道:当你旅行的时候。会以一种实在的方式体验到再生的过程。你会遇到全新的环境,时间也因此变得缓慢。而且在大多数时候,你甚至不知道那里的语言,所以在旅行时,你就像一个刚刚离开子宫的孩子。
⑥人类学家在讲述人生礼仪时,把它当作一种“转变的仪式”,当仪式结束,参与者便完成了身份的转变。非洲部落里的少年,总是独自一人被驱赶着走进草原,当他们筋疲力尽地归来时,便完成了自身的“成年礼”。人类学家特纳曾指出,这个过程让你从熟悉的环境里走出来,在仪式中经历嬗变。这应该是种混沌、模糊、而又异常神圣的情绪,它让一个人在内心矛盾与时光的消逝中迎接新生。
⑦无论是部落里的少年,还是群岛上的土著,他们都是在陌生的环境里体会生命的冲动。这就好像那些朝圣者,每每从熟悉的生活里走出。当“朝觐(cháojìn,指宗教徒拜谒圣像、圣地等)之旅”开始时,他们便摆脱了与过去的纠缠。这些人披荆斩棘、历尽艰难,在漫长的隐忍后,终于实现了灵魂的重生。这样的朝圣必然是一场孤独、倔强,甚至有些残酷的蜕变过程,如凤凰涅槃(nièpán,指佛教用语,指超脱生死的境界),浴火而生。
⑧人类朝圣和旅行,有着结构上的相似,它们都是和旧有生活的告别,同样在行走中期待着新生。人们在内心动力的驱使下,开始去寻找异己的世界,这种寻找有时有几分偏执。缘于对重生的那份热切的渴望。而仿佛只有在差异中,我们才能不断实现对自身的反省。由此来看,当我们不断地踏上旅途,把自己置身于异乡陌生的环境时,旅行之于我们,其实是一场人生的朝圣。
【小题1】⑴题目“行走的成年礼”中“行走”指什么?(2分)
⑵题目中包含了作者怎样的观点?(2分)
【小题2】文章第①段提到“我”在拉萨遇到朋友的事,是要说明什么?(3分)
【小题3】“我”喜欢旅行的原因有哪些?请用原文的语句回答。(4分)
【小题4】.为什么作者认为“旅行之于我们,其实是一场人生的朝圣”?(4分)
【小题5】有关旅行,日本著名哲学家三木清说:“旅行是人生的缩影。因为在旅行时脱离了日常的事物而陷入纯粹的静观,对于以平生自明的、已知的事理为前提的人,才保持了新鲜的感觉。旅行能体味人生。”你怎么看旅行?结合生活实际,说说你的看法。(不少于80字)(6分) 查看习题详情和答案>>
(1)为了节约原料,硫酸和硝酸的物质的量之比最佳为: ;为了吸收该反应中产生的尾气,请选择下列中合适的装置 。
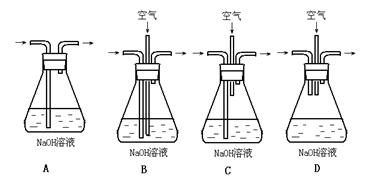
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH ,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
已知:Ksp[Cu((OH)2]≈10-22, Ksp[Fe((OH)2]≈10-16, Ksp[Fe((OH)3]≈10-38
请回答下列问题:
如开始加入的铜粉为3.2 g,最后所得溶液为500 mL,溶液中含有铁元素0.005 mol。
①方案1中的B仪器名称是 。
②为了使铁元素全部沉淀,应调节pH至少为_________。
③方案2中甲物质可选用的是 。
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E、Fe2(SO4)3 |
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45 mL 1.5mol·L-1的稀硫酸中,控温在50℃。加入18mL 10%的H2O2,反应0.5h,升温到60℃,持续反应1 h后,过滤、蒸发浓缩、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 10.5g。
请回答下列问题:
⑤反应时温度控制在50℃~60℃不宜过高的原因是 ,
⑥本实验CuSO4·5H2O的产率为 。 查看习题详情和答案>>
根据情景提示,用恰当的短语或句子填空。(每空2分,共10分)
* 你想建议同学Jim加入英语俱乐部,你可以这样说:
1.Maybe _______________________________________________________ , Jim!
* 你想告诉朋友“你过去很怕黑”,你可以这样说:
2._______________________________________________________________.
* 你想知道对方怎样准备考试的,你该怎么问:
3.
* 你想知道如果Jack有一百万元,他将会怎么做?你可以这样问他:
4. if you had a million dollars, Jack?
*它一定属于卡拉的。
5.It __________________________Carla.
查看习题详情和答案>>
完成句子 按所给的汉语,用英语完成下列句子。
【小题1】就如何处理这件事情,我给他们提了一些建议。
I provided them it.
【小题2】尽管他是个百万富翁,但他已把一生都献给帮助残疾人。
Although he is a millionaire, the disabled.
【小题3】我相信机器人不会对我们的日常生活构成很大的不同。
I our everyday life.
【小题4】我表妹问压缩食品是否可以储藏很久。
My cousin asked or not.
【小题5】雪下得太大了,使得我们没法去听音乐会。
The snow was going to the concert.
【小题6】与小说相比,网络游戏对我们学生有不良影响。
novels, online games us students.
根据所给提示将下列句子译成英语。(共5小题,每题2分,满分10分)
1.公园就在超市的左边。
The park is ______ the ______ of the supermarket.
2.Lily 擅长英语
Lily is ________________English.
3.我的老师带着眼镜。
My teacher _______ ________.
4.你们班有多少学生?
__________________ students are there in your class?
5.他们来自北京吗?
Do they ________ ______ Beijing ?
查看习题详情和答案>>