网址:http://m.1010jiajiao.com/timu_id_125777[举报]
选择题(本题包括8小题。每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分,共48分。)
题号
14
15
16
17
18
19
20
21
答案
D
D
A
B
D
B
BD
C
22.(1)①113~115都对
②6.5×10-10―6.6×10-10都对
③这样做的目的是为了让油膜在水平面上形成单分子油膜
(2)① >(4分); ②灵敏电流计(4分); ③ 2(4分)
23.(16分)(1)根据牛顿第二定律,滑块相对车滑动时的加速度
 (1分)
(1分)
滑块相对车滑动的时间  (1分)
(1分)
滑块相对车滑动的距离  (2分)
(2分)
滑块与车摩擦产生的内能  (2分)
(2分)
由上述各式解得  (与动摩擦因数μ无关的定值) (2分)
(与动摩擦因数μ无关的定值) (2分)
(2)设恒力F取最小值为F1,滑块加速度为a1,此时滑块恰好到达车的左端,则
滑块运动到车左端的时间  ① (1分)
① (1分)
由几何关系有  ② (2分)
② (2分)
由牛顿定律有  ③ (2分)
③ (2分)
由①②③式代入数据解得  ,
, (2分)
(2分)
则恒力F大小应该满足条件是  (1分)
(1分)
 24.解:(1)
24.解:(1)  =
=  ……………………………① 1分
……………………………① 1分
 =
=
I=  ………………………………③ 1分
………………………………③ 1分
由⑴,⑵,⑶得  ……………④ 1分
……………④ 1分
(2)AB棒滑到DF处时
 …………………⑤ 1分
…………………⑤ 1分
 ……………………⑥
2分
……………………⑥
2分
 ……………⑦
2分
……………⑦
2分
由⑸⑹⑺得  ………………⑧
1分
………………⑧
1分
(3)电机做的功 ………………⑨ 2分
………………⑨ 2分
 ?……⑩ 1分
?……⑩ 1分
 是AB棒在DEF上滑动时产生的电热,数值上等于克服安培力做的功
是AB棒在DEF上滑动时产生的电热,数值上等于克服安培力做的功
 ………………………………………………⑾ 1分
………………………………………………⑾ 1分
 又
又  ,
,
故 ……………⑿
2分
……………⑿
2分
 是AB棒在CDFG导轨上滑动时产生的电热,电流恒定,电阻不变
是AB棒在CDFG导轨上滑动时产生的电热,电流恒定,电阻不变
 ………………⒀ 1分
………………⒀ 1分
由⑼、⑽、⑿、⒀得  …………⒁ 1分
…………⒁ 1分
25.(1)要使小球在竖直平面内做匀速圆周运动,必须满足 (2分)
(2分)
所以  =2×103N/C (2分) 方向竖直向上(1分)
=2×103N/C (2分) 方向竖直向上(1分)
(2)由功能关系得,弹簧具有的最大弹性势能
 (2分)
(2分)
设小球 运动到
运动到 点时速度为
点时速度为 ,由功能关系得
,由功能关系得 (2分)
(2分)
 (1分)
(1分)
两球碰后结合为 ,设
,设 的速度为
的速度为 ,
,
由动量守恒定律得 
 (2分)
(2分)
(3)加电场后,因


 所以
所以 不能做圆周运动,而是做类平抛运动,设经过时间
不能做圆周运动,而是做类平抛运动,设经过时间 绳子在Q处绷紧,由运动学规律得
绳子在Q处绷紧,由运动学规律得


 可得
可得 


即:绳子绷紧时恰好位于水平位置,水平方向速度变为0,以竖直分速度 开始做圆周运动(2分)
开始做圆周运动(2分)
设到最高点时速度为 由动能定理得;
由动能定理得;
 (2分)
(2分)
得 (1分)
(1分)
在最高点由牛顿运动定律得; (2分)
(2分)
求得  (1分)
(1分)
化学试题参考答案
选择题(本题包括8道小题,每小题只有一个选项符合题意;每小题6分,共48分)
题号
6
7
8
9
10
11
12
13
答案
A
C
B
A
C
B
C
C
26.(每空2分,共12分)
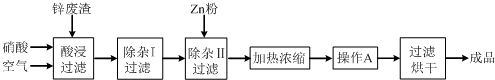
⑴①加适量水溶解,搅拌,过滤。
②使Fe3+可全部转化为Fe(OH)3沉淀,而Cu2+不会转化为Cu (OH)2沉淀。
③将CuSO4?5H2O溶液加热蒸发至有晶膜出现时,停止加热。受热均匀,温度易于控制在
⑵ ①CuO可加快H2O2分解的反应速率,是H2O2分解反应的催化剂。
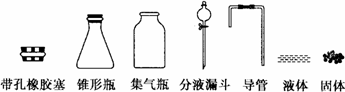
② 秒表、橡皮塞、导管、集气瓶、量筒。
27.(每空2分,共12分)
(1)① (如右图配置)
(如右图配置)
②打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加。
(2)①溶液褪色 ②溶液褪色 ③有浅黄色沉淀(或溶液变浑浊)
(3)①Na2SO3变质 取待测的试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液有白色沉淀生成,则证明该Na2SO3固体变质;
②不是浓硫酸 用洁净玻璃棒蘸取待测的试样,涂白纸不变黑,则证明该溶液不是浓硫酸。
28. 每空2分,共14分)
(1) Fe3O4 电子式:略

 CH2 =C(CH3)―CH=CH2 +2NaBr +2H2O。
CH2 =C(CH3)―CH=CH2 +2NaBr +2H2O。