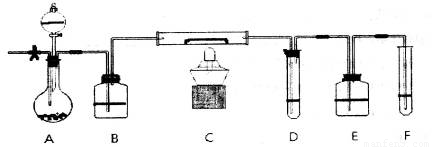
摘要:(1)如何检查装置A的气密性: . (2)装置A发生的反应有时要向其中加入少量硫酸铜溶液.其目的是 . (3)为了安全.在点燃D处的酒精灯之前.在b出口处必须 . (4)装置B的作用是 .装置C中装的液体是 .所起的作用是 . (5)在气密性完好.并且进行了必要的安全操作后.点燃D处的酒精灯.在硬质双通玻璃管中发生的化学反应方程式是: .
网址:http://m.1010jiajiao.com/timu_id_116483[举报]
1.(16分)
(1)①洗去油污(1分);③在②的滤液中加入稍过量的洗涤过的废铁屑,充分反应后过滤(1分);④将③的滤渣溶入足量的稀硫酸中,过滤,滤液保留待用(1分);(2)⑤、③(1分),将溶液加热到
(3)否(1分),普通自来水中含Cl―,使Ag+被沉淀(1分)。 (共2分)
(4)Fe+2Ag+
Fe2++2Ag,Fe2O3+6H+ 2Fe3++3H2O,Fe+2Fe3+ 3Fe2+,
Fe+2H+ Fe2++H2↑
(各1分,共4分)
(5)抑制Fe2+的水解,防止Fe2+被氧化 (2分)
2.(10分)(1)MnO2, NaOH溶液 (各1分) (共2分)
(2)2NaOH+Cl2==== NaCl+NaClO+H2O (2分)
(3)①不能(1分),HCl气体进入C中,消耗NaOH, 降低NaClO的纯度。(2分)(共3分)




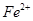 ,如何检验含有Fe2+____________________________________。
,如何检验含有Fe2+____________________________________。
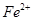 ,如何检验含有Fe2+____________________________________。
,如何检验含有Fe2+____________________________________。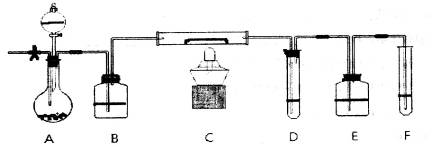
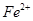 ,如何检验含有Fe2+____________________________________。
,如何检验含有Fe2+____________________________________。
 s
s ________。
________。