摘要:把质量为5g是CuO和炭粉混合物加热至不再生成红色物质为止.冷却后分离.得到3.2g红色物质.求原混合物中CuO的质量分数.
网址:http://m.1010jiajiao.com/timu3_id_99969[举报]
有一包黑色粉末,可能含有氧化铜、铁粉和炭粉中的一种或三种,课外小组为了探究其成分,进行了探究.请你帮助他们完成下列实验报告:
查看习题详情和答案>>
| 实验操作 | 实验现象 | 实验结论 |
| (1)将固体溶于足量的 硫酸 硫酸 溶液中 |
有气泡产生,黑色粉末全部溶解,有红色固体生成并得到澄清、透明溶液 | 该固体的成分是: 铁和氧化铜 铁和氧化铜 |
| (2) 将固体溶于足量的 将固体溶于足量的 稀硫酸中 稀硫酸中 |
没有气泡产生, 没有气泡产生, 黑色粉末部分溶解, 黑色粉末部分溶解, 并得到澄清、透明蓝色溶液 并得到澄清、透明蓝色溶液 |
该固体是CuO和炭粉的混合物 |
| (3) 将固体溶于足量的 将固体溶于足量的 稀硫酸中 稀硫酸中 |
黑色粉末不溶解 | 该固体的成分是: 炭粉 炭粉 |
有一包黑色粉末,可能含有氧化铜、铁粉和炭粉中的一种或三种,课外小组为了探究其成分,进行了探究.请你帮助他们完成下列实验报告:
查看习题详情和答案>>
| 实验操作 | 实验现象 | 实验结论 |
| (1)将固体溶于足量的 ______溶液中 | 有气泡产生,黑色粉末全部溶解,有红色固体生成并得到澄清、透明溶液 | 该固体的成分是: ______ |
| (2)______ ______ | ______ ______ ______ | 该固体是CuO和炭粉的混合物 |
| (3)______ ______ | 黑色粉末不溶解 | 该固体的成分是: ______ |
查看习题详情和答案>>
有一包黑色粉末,可能含有氧化铜、铁粉和炭粉中的一种或三种,课外小组为了探究其成分,进行了探究.请你帮助他们完成下列实验报告:
查看习题详情和答案>>
| 实验操作 | 实验现象 | 实验结论 |
| (1)将固体溶于足量的 ______溶液中 |
有气泡产生,黑色粉末全部溶解,有红色固体生成并得到澄清、透明溶液 | 该固体的成分是: ______ |
| (2)______ ______ |
______ ______ ______ |
该固体是CuO和炭粉的混合物 |
| (3)______ ______ |
黑色粉末不溶解 | 该固体的成分是: ______ |
 (2008?遵义)碱式碳酸铜[化学式Cu2(OH)2CO3,相对分子质量为222]加热完全分解后生成的黑色固体是什么?甲、乙、丙、丁四位同学对此进行探究.请你与他们一起,踏上探究之路.
(2008?遵义)碱式碳酸铜[化学式Cu2(OH)2CO3,相对分子质量为222]加热完全分解后生成的黑色固体是什么?甲、乙、丙、丁四位同学对此进行探究.请你与他们一起,踏上探究之路.(1)他们称取了2.5g碱式碳酸铜在试管中加热使之完全分解,冷却至室温后,称量黑色固体产物质量为1.8g.结合碱式碳酸铜的化学式,他们对黑色固体产物做出以下猜想:
a、可能是氧化铜; b、可能是炭粉; c、可能是氧化铜和炭粉的混合物.他们做出以上猜想的依据是
化学反应前后元素种类不变且氧化铜和炭粉都是黑色固体
化学反应前后元素种类不变且氧化铜和炭粉都是黑色固体
.(2)甲同学从资料中得知:碳、氢气、一氧化碳在加热或高温条件下都能夺取一些金属氧化物中的氧,使其变为金属单质.他认为猜想C可以排除,理由是
炭粉与氧化铜在加热或高温的条件下能发生反应
炭粉与氧化铜在加热或高温的条件下能发生反应
.(3)乙同学通过对得到的实验数据进行计算分析.排出了猜想b,他的理由是
2.5g×
≈0.14g<1.8g碱式碳酸铜中碳元素质量小于黑色固体的质量
| 12 |
| 222 |
2.5g×
≈0.14g<1.8g碱式碳酸铜中碳元素质量小于黑色固体的质量
.| 12 |
| 222 |
(4)黑色固体究竟是什么?
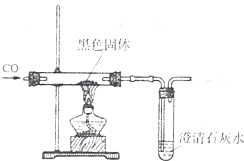
丙同学设计的实验方案:向盛有少量该黑色固体的试管中加入足量的稀硫酸,充分振荡后,静置观察.黑色固体消失,溶液变蓝.丁同学设计的实验方案(如右图所示):在盛有少量该黑色固体的玻璃管中,通入一氧化碳后加热.黑色固体逐渐变成光亮的红色,澄清石灰水变浑浊.他们根据实验现象都得出结论:黑色固体是氧化铜.丙、丁两同学的实验方案,
丙同学
丙同学
(填丙同学或丁同学)较好,谈谈你的看法:
丁同学方案需加热或操作复杂或易污染空气等
丁同学方案需加热或操作复杂或易污染空气等
.(简答一条)(5)科学探究的方法和途径有多种,只要善于思考,就会有惊喜的发现.根据实验数据进行计算分析,也可以得出结论:黑色固体是氧化铜.理由是
设2.5g碱式碳酸铜能得到氧化铜的质量为x,根据质量守恒
Cu2(OH)2CO3~2CuO
=
x≈1.8g与生成黑色固体的质量相等,则黑色固体产物为氧化铜.
或2.5g碱式碳酸铜可转化为CuO的质量为:2.5g×
÷
≈1.8g与生成黑色固体质量相等,则黑色固体产物为氧化铜.
Cu2(OH)2CO3~2CuO
| 222 |
| 2.5g |
| 2×80 |
| x |
或2.5g碱式碳酸铜可转化为CuO的质量为:2.5g×
| 2×64 |
| 222 |
| 64 |
| 80 |
设2.5g碱式碳酸铜能得到氧化铜的质量为x,根据质量守恒
Cu2(OH)2CO3~2CuO
=
x≈1.8g与生成黑色固体的质量相等,则黑色固体产物为氧化铜.
或2.5g碱式碳酸铜可转化为CuO的质量为:2.5g×
÷
≈1.8g与生成黑色固体质量相等,则黑色固体产物为氧化铜.
.Cu2(OH)2CO3~2CuO
| 222 |
| 2.5g |
| 2×80 |
| x |
或2.5g碱式碳酸铜可转化为CuO的质量为:2.5g×
| 2×64 |
| 222 |
| 64 |
| 80 |
(2004?扬州)某黑色物质可能是CuO、C中的一种或两种,小宇同学为研究该黑色物质,设计如下方案(若有C存在,含量较少):
研究成分:小宇同学设计的两个实验方案如下:
甲:黑色粉末
观察溶液颜色观察现象;
乙:黑色粉末
产物与白色硫酸铜接触
观察现象.
试回答:
(1)甲方案中证明有氧化铜的实验现象是
(2)乙方案中仅有氧化铜的实验现象是
(3)以上两个方案中,你认为哪个方案更好,理由是什么?
(4)问题讨论:
经过查阅资料:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O.
若黑色物质中有Cu,使用甲方案,并将盐酸改为稀硫酸,并加热较长时间,是否可行?
研究组成:若小宇经实验证明该黑色固体是CuO和C的混合物,则根据上述两个方案,补充相应步骤,以确定其中氧化铜的质量分数,请帮助他完成下表.(该混合物质量已经测定)
查看习题详情和答案>>
研究成分:小宇同学设计的两个实验方案如下:
甲:黑色粉末
| ||
| 微热 |
乙:黑色粉末
| ||
| 并加热 |
| ||
| 澄清石灰水 |
试回答:
(1)甲方案中证明有氧化铜的实验现象是
溶液呈现蓝色
溶液呈现蓝色
,证明有炭粉的实验现象是溶液底部有黑色物质
溶液底部有黑色物质
.(2)乙方案中仅有氧化铜的实验现象是
白色硫酸铜变蓝且澄清石灰水不变浑浊
白色硫酸铜变蓝且澄清石灰水不变浑浊
.(3)以上两个方案中,你认为哪个方案更好,理由是什么?
甲方案好,简便节能
甲方案好,简便节能
(4)问题讨论:
经过查阅资料:Cu+2H2SO4(浓)
| ||
若黑色物质中有Cu,使用甲方案,并将盐酸改为稀硫酸,并加热较长时间,是否可行?
不可行
不可行
(填行或不行).理由是加热较长时间后的稀硫酸变成浓硫酸,铜也能与之反应产生蓝色现象,会干扰CuO的鉴定
加热较长时间后的稀硫酸变成浓硫酸,铜也能与之反应产生蓝色现象,会干扰CuO的鉴定
.研究组成:若小宇经实验证明该黑色固体是CuO和C的混合物,则根据上述两个方案,补充相应步骤,以确定其中氧化铜的质量分数,请帮助他完成下表.(该混合物质量已经测定)
| 方案 | 方案中所发生的 化学方程式 |
实验所用仪器 (各缺一件玻璃仪器,填完整) |
实验需要 测定的物理量 |
| 甲 | CuO+2HCl=CuCl2+H2O CuO+2HCl=CuCl2+H2O |
托盘天平、烧杯、试管、酒精灯、 玻璃棒、 漏斗 漏斗 . |
过滤洗涤干燥后的碳的质量 过滤洗涤干燥后的碳的质量 |
| 乙 | 启普发生器、托盘天平、硬质试管、U型管、 玻璃导管、广口瓶、 酒精灯 酒精灯 . |
反应前U型管及其中硫酸铜总质量及 反应后U型管的总质量 反应后U型管的总质量 |