摘要:PH的范围通常在 之间.测定溶液的PH常用
网址:http://m.1010jiajiao.com/timu3_id_99785[举报]
检验溶液的酸碱性可以使用
______,溶液的酸碱度可用______来表示,粗略测定溶液的pH可以使用____,要精确地测定溶液的pH可以使用______.pH的范围通常在_____之间.pH=0的溶液是____性溶液,pH=14的溶液是_____性溶液. 查看习题详情和答案>>检验溶液的酸碱性可以使用
______,溶液的酸碱度可用______来表示,粗略测定溶液的pH可以使用____,要精确地测定溶液的pH可以使用______.pH的范围通常在_____之间.pH=0的溶液是____性溶液,pH=14的溶液是_____性溶液. 查看习题详情和答案>>
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标.某兴趣小组同学收集某地的雨水进行实验.
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
②SO2能使品红溶液褪色;
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为 .
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于 .
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式 .
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质 .
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加 溶液,溶液呈 色.证明在酸雨样品中滴加的Ba(OH)2溶液已过量.
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为 ,根此现象有关酸雨中溶质的猜想 正确.
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为 .
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为 .
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:
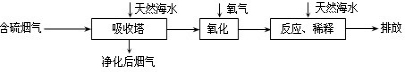
天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案: .
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是 .
查看习题详情和答案>>
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:

天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案:
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标.某兴趣小组同学收集某地的雨水进行实验.
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为________.
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于________.
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式________.
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质________.
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加________溶液,溶液呈________色.证明在酸雨样品中滴加的Ba(OH)2溶液已过量.
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为________,根此现象有关酸雨中溶质的猜想________正确.
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为________.
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为________.
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:
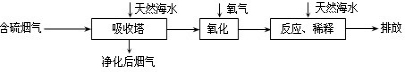
天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案:________.
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是________. 查看习题详情和答案>>
(2011?如皋市一模)酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标.某兴趣小组同学收集某地的雨水进行实验.
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
②SO2能使品红溶液褪色;
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为______.
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于______.
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式______.
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质______.
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加______溶液,溶液呈______色.证明在酸雨样品中滴加的Ba(OH)2溶液已过量.
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为______,根此现象有关酸雨中溶质的猜想______正确.
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为______.
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为______.
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:
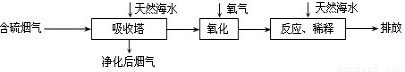
天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案:______.
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
查看习题详情和答案>>
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
| 测定时间/h | 1 | 2 | 3 | 4 | |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为______.
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于______.
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式______.
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质______.
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加______溶液,溶液呈______色.证明在酸雨样品中滴加的Ba(OH)2溶液已过量.
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为______,根此现象有关酸雨中溶质的猜想______正确.
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为______.
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为______.
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:

天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案:______.
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
查看习题详情和答案>>