摘要:3.⑴CuO+H2SO4=CuSO4+H2O ⑵40% ⑶9.8%
网址:http://m.1010jiajiao.com/timu3_id_99605[举报]
兴趣小组的同学在开展“废物利用、减少污染”的活动中,取某工厂合金废料(含铝、铁、铜)进行如图实验:

(1)操作Ⅰ的名称是
(2)固体A的成分是
(3)黑色固体C加适量稀硫酸反应的方程式为
查看习题详情和答案>>

(1)操作Ⅰ的名称是
过滤
过滤
;该操作需用到的铁制仪器为铁架台
铁架台
.(2)固体A的成分是
铁和铜
铁和铜
;操作Ⅱ反应的化学方程式为Fe+H2SO4 ═FeSO4+H2↑
Fe+H2SO4 ═FeSO4+H2↑
.(3)黑色固体C加适量稀硫酸反应的方程式为
CuO+H2SO4═CuSO4+H2O
CuO+H2SO4═CuSO4+H2O
.29、以下框图中的物质除乙外均为初中化学中的常见物质,其中D、E、H、丙均为单质,甲为无色的液体燃料,C可使澄清石灰水变浑浊,D是最清洁的燃料,G的水溶液呈蓝色.
(1)写出甲和F的化学式:甲
(2)乙中肯定含有的原子团是
(3)写出F→G的化学方程式:
(4)现用以下装置进行实验,确证甲燃烧的三种产物,则需要连接的装置顺序为:

查看习题详情和答案>>

(1)写出甲和F的化学式:甲
C2H5OH
F
CuO
(2)乙中肯定含有的原子团是
CO32-(或HCO3-)
(写离子符号);C→B基本反应类型是
化合反应
;(3)写出F→G的化学方程式:
CuO+H2SO4=CuSO4+H2O
.(4)现用以下装置进行实验,确证甲燃烧的三种产物,则需要连接的装置顺序为:
A
接
D
接
C
接
B
接
E
接
D
.(仪器可以重复使用,填写装置编号,尾气吸收装置已省略,装置中药品均过量).
A为黑色固体,A、C、D、Y都是氧化物,E是单质,F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系.请回答:
信息:CuO+H2SO4=CuSO4+H2O
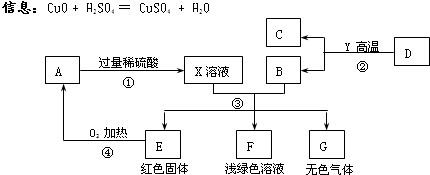
(1)X溶液中所含有的溶质为 ,固体A的化学式为 ,F溶液显浅绿色,其中所含有的溶质是 .
(2)写出反应②的化学方程式 ,
(3)写出反应③中生成无色气体的化学方程式 ,
(4)指出物质G和A在加热条件下发生的化学反应的基本反应类型 .
查看习题详情和答案>>
信息:CuO+H2SO4=CuSO4+H2O

(1)X溶液中所含有的溶质为
(2)写出反应②的化学方程式
(3)写出反应③中生成无色气体的化学方程式
(4)指出物质G和A在加热条件下发生的化学反应的基本反应类型
现有NaOH 溶液、CuO、Fe、稀 H2SO4、CuSO4溶液五种物质,圈圈相连的物质间能发生化学反应,已知E的粉末通常为黑色.回答下列问题:
(1)将所给五种物质填入圈内;
(2)写出B、C反应的化学方程式
(3)D、E恰好完全反应的实验现象

查看习题详情和答案>>
(1)将所给五种物质填入圈内;
(2)写出B、C反应的化学方程式
CuO+H2SO4═CuSO4+H2O
CuO+H2SO4═CuSO4+H2O
(3)D、E恰好完全反应的实验现象
有红色固体生成,溶液由蓝色变为浅绿色
有红色固体生成,溶液由蓝色变为浅绿色

碱式碳酸铜是一种绿色的固体,受热分解成黑色固体物质、二氧化碳和水.这种黑色固体的成分是什么呢?亮亮与间学们进行以下探究:
[猜想]:该黑色固体可能氧化铜,也可能是氧化铜和炭的混合物.
[设计与实验]
接着小明与同学们用氢气还原氧化铜制取铜.
(1)要制得纯净的氢气,小明应选用的药品是
A、铁和稀硫酸 B、锌和浓盐酸 C、镁和稀硫酸D、锌和稀硫酸
(2)实验开始时,应先通入一会儿
(3)实验结束后,小方同学对还原后的红色物质产生了兴趣,该红色物质一定是单质铜吗?
查阅有关资料获知:氢气与氧化铜在加热条件下能生成氧化亚铜(Cu2O),氧化亚铜也呈红色,且能与稀硫酸反应生成硫酸铜、铜和水.
为此,小方同学靠后做了两次实验,第一次称取4.0g氧化铜进行实验,得到了3.3g红色物质;第二次同样用4.0g氧化铜进行实验,得到了3.2g红色物质.
①小方通过对所得实验数据迸行计算分析后知t第二次实验得到的红色物质全部是铜,第一次得到的红色物质除铜外,还含有氧化亚铜.小方的分析依据是
②随后,他用化学实验方法验证了上述分析结果的正确性.其验证方法是(简要写出操作现象、结论)
③从上述实验中,小方获得以下结论:在氢气还原氧化铜实验中,若还原不充分,一会得到红色氧化亚铜,请写出氢气还原氧化铜生成氧化亚铜的化学方程式
查看习题详情和答案>>
[猜想]:该黑色固体可能氧化铜,也可能是氧化铜和炭的混合物.
[设计与实验]
| 实验步骤 | 实验现象 | 结论和化学方程式 |
| 亮亮同学取少量黑色固体,放入试管中,加入足量的稀硫酸,微热. | 黑色固体完全消失,溶液变 蓝 蓝 色. |
此黑色固体是氧化铜.该反应的化学方程式为 CuO+H2SO4═CuSO4+H2O CuO+H2SO4═CuSO4+H2O |
(1)要制得纯净的氢气,小明应选用的药品是
D
D
A、铁和稀硫酸 B、锌和浓盐酸 C、镁和稀硫酸D、锌和稀硫酸
(2)实验开始时,应先通入一会儿
H2
H2
,然后再加热,这样操作的目的是防止加热时发生爆炸
防止加热时发生爆炸
(3)实验结束后,小方同学对还原后的红色物质产生了兴趣,该红色物质一定是单质铜吗?
查阅有关资料获知:氢气与氧化铜在加热条件下能生成氧化亚铜(Cu2O),氧化亚铜也呈红色,且能与稀硫酸反应生成硫酸铜、铜和水.
为此,小方同学靠后做了两次实验,第一次称取4.0g氧化铜进行实验,得到了3.3g红色物质;第二次同样用4.0g氧化铜进行实验,得到了3.2g红色物质.
①小方通过对所得实验数据迸行计算分析后知t第二次实验得到的红色物质全部是铜,第一次得到的红色物质除铜外,还含有氧化亚铜.小方的分析依据是
4gCuO中含有的铜元素质量为3.2g,所以生成铜的质量为3.2g
4gCuO中含有的铜元素质量为3.2g,所以生成铜的质量为3.2g
.②随后,他用化学实验方法验证了上述分析结果的正确性.其验证方法是(简要写出操作现象、结论)
分别取两种红色固体于试管中,加入稀硫酸.第一次试管中溶液变蓝,第二次试管中溶液不变蓝,则第一次的产物中含有氧化亚铜,第二次的是铜
分别取两种红色固体于试管中,加入稀硫酸.第一次试管中溶液变蓝,第二次试管中溶液不变蓝,则第一次的产物中含有氧化亚铜,第二次的是铜
③从上述实验中,小方获得以下结论:在氢气还原氧化铜实验中,若还原不充分,一会得到红色氧化亚铜,请写出氢气还原氧化铜生成氧化亚铜的化学方程式
2CuO+H2
Cu2O+H2O
| ||
2CuO+H2
Cu2O+H2O
.
| ||