摘要:找到突破口进行联想,2.在训练中找感觉.
网址:http://m.1010jiajiao.com/timu3_id_9931[举报]
在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中不断地吹气,在吹气的过程中发现石灰水先出现浑浊后又变澄清,他感到很意外.
小强又将纯净的CO2持续通入新制的澄清石灰水中,一段时间后,观察到的现象与上次相同.
(1)小强做第二次实验的目的是_____________________.
(2)小强从老师那里得知:CO2能与CaCO3和H2O继续反应生成Ca(HCO3)2.由此小强推测出Ca(HCO3)2的一条物理性质是______________________.
小强还想了解Ca(HCO3)2的化学性质.
[提出猜想]Ca(HCO3)2受热能否分解?
[查阅资料]Ca(HCO3)2受热分解生成CaCO3、H2O和CO2.
[设计实验]小强用下图所示装置进行实验,加热时通过检验产物中有水和二氧化碳生成,就可证明Ca(HCO3)2受热能分解.
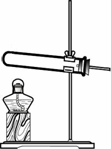
[实验过程]小强在实验室找到一瓶Ca(HCO3)2粉末,取出少量放入试管中进行加热,观察到试管口附近有小液滴产生.小强得出结论:Ca(HCO3)2受热能分解.
[反思和评价]
小松认为小强的实验不能证明Ca(HCO3)2受热一定分解了,小松的理由是______________.
[进一步实验]请你通过实验,验证加热Ca(HCO3)2过程中有CO2产生(填写下表中实验操作及现象).

(1)实验室制取二氧化碳时不选用稀硫酸替代稀盐酸的原因是
(2)使用氢气时要特别注意安全.点燃氢气等可燃性气体前,一定要
查看习题详情和答案>>
硫酸溶液与大理石反应成微溶的硫酸钙,阻止反应进一步进行
硫酸溶液与大理石反应成微溶的硫酸钙,阻止反应进一步进行
.(2)使用氢气时要特别注意安全.点燃氢气等可燃性气体前,一定要
验纯
验纯
.利用铝土矿(只考虑含Al2O3及Fe2O3)生产Al的工艺流程如下,请回答下列问题:
[查阅资料]:
1、铝土矿中Al2O3可以和NaOH溶液反应,反应的化学方程式为:Al2O3+2NaOH═2NaAlO2+2H2O;
2、Fe2O3不和NaOH溶液反应.
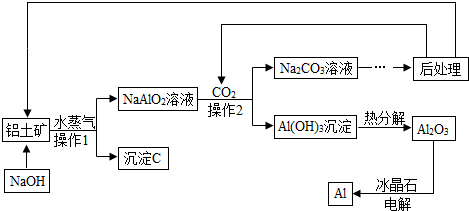
(1)工业生产中,要将铝土矿细磨预处理,目的是
(2)沉淀C的化学式是
(3)操作1、操作2的名称是
(4)此工艺中,可循环使用的物质是CO2、H2O和
(5)电解Al2O3的化学方程式为
(6)NaAlO2溶液中通入CO2反应的化学方程式是
查看习题详情和答案>>
[查阅资料]:
1、铝土矿中Al2O3可以和NaOH溶液反应,反应的化学方程式为:Al2O3+2NaOH═2NaAlO2+2H2O;
2、Fe2O3不和NaOH溶液反应.

(1)工业生产中,要将铝土矿细磨预处理,目的是
增加反应物接触面积,使反应充分进行
增加反应物接触面积,使反应充分进行
;(2)沉淀C的化学式是
Fe2O3
Fe2O3
;(3)操作1、操作2的名称是
过滤
过滤
,实验室完成此操作时,需要的玻璃仪器的是玻璃棒、烧杯和漏斗
漏斗
;(4)此工艺中,可循环使用的物质是CO2、H2O和
NaOH
NaOH
;(填化学式)(5)电解Al2O3的化学方程式为
2Al2O3
4Al+3O2↑
| ||
2Al2O3
4Al+3O2↑
;
| ||
(6)NaAlO2溶液中通入CO2反应的化学方程式是
2NaAlO2+CO2+3H2O═Na2CO3+2Al(OH)3↓
2NaAlO2+CO2+3H2O═Na2CO3+2Al(OH)3↓
.(2005?防城港)广西有大量的石灰石,为了测定某地石灰石中碳酸钙的质量分数(假设杂质不参加反应,且不溶于水),某兴趣小组的同学设计了三个实验方案并进行了如下探究:
方案I:①称取石灰石样品10g②高温煅烧至质量不再改变,然后把剩余固体放在密闭干燥的容器中冷却至室温,称得剩余固体质量为6.04g.
方案Ⅱ:①称取石灰石样品10g ②加入足量的质量分数为10%的稀盐酸100g,使碳酸钙完全溶解 ③过滤后在滤液中加入过量的质量分数为15%的碳酸钠溶液150g④将步骤③中的沉淀过滤、洗涤、干燥,称得沉淀质量为9g.
方案Ⅲ:①称取石灰石样品lO g②加入足量的稀盐酸,使碳酸钙全部溶解
③用导管将生成的气体通入澄清石灰水(过量) ④将步骤③中生成的沉淀过滤、洗涤、干燥,称得沉淀质量为8.8g.
根据上述回答问题:
(1)在方案I中冷却剩余固体为什么要在密闭干燥的容器中进行?
(2)某同学根据方案I计算碳酸钙的质量分数过程如下:设石灰石中碳酸钙的质量为X,则
CaCO3
CaO+CO2↑
100 56
x 6.04g
=
x=lO.78g
CaCO3%=
×100%=107.8%
以上解法得出碳酸钙的质量分数超过100%,造成计算结果错误的原因是
(3)方案Ⅱ中求碳酸钙的质量分数时,下列数据不需要的是
A.10%、100g B.10g C.15%、150g D.9g
(4)通过对三个方案中的碳酸钙质量分数的计算可知,方案Ⅲ计算得出的碳酸钙质量分数要比方案工和方案Ⅱ低,你认为其中可能的原因是下面的
A.生成的二氧化碳有部分溶于水 B.导管中仍有部分二氧化碳未排出.
C.生成的沉淀不应该洗涤和干燥 D.稀盐酸不应加足量
(5)请你另外设计一个实验方案,测定石灰石中碳酸钙的质量分数.(提示:可以从求杂质的角度来分析)
查看习题详情和答案>>
方案I:①称取石灰石样品10g②高温煅烧至质量不再改变,然后把剩余固体放在密闭干燥的容器中冷却至室温,称得剩余固体质量为6.04g.
方案Ⅱ:①称取石灰石样品10g ②加入足量的质量分数为10%的稀盐酸100g,使碳酸钙完全溶解 ③过滤后在滤液中加入过量的质量分数为15%的碳酸钠溶液150g④将步骤③中的沉淀过滤、洗涤、干燥,称得沉淀质量为9g.
方案Ⅲ:①称取石灰石样品lO g②加入足量的稀盐酸,使碳酸钙全部溶解
③用导管将生成的气体通入澄清石灰水(过量) ④将步骤③中生成的沉淀过滤、洗涤、干燥,称得沉淀质量为8.8g.
根据上述回答问题:
(1)在方案I中冷却剩余固体为什么要在密闭干燥的容器中进行?
(2)某同学根据方案I计算碳酸钙的质量分数过程如下:设石灰石中碳酸钙的质量为X,则
CaCO3
| ||
100 56
x 6.04g
| 100 |
| x |
| 56 |
| 6.04g |
CaCO3%=
| 10.78 |
| 10 |
以上解法得出碳酸钙的质量分数超过100%,造成计算结果错误的原因是
剩余固体质量6.04g包括了杂质的质量
剩余固体质量6.04g包括了杂质的质量
,正确的计算结果是90%
90%
.(3)方案Ⅱ中求碳酸钙的质量分数时,下列数据不需要的是
AC
AC
(填序号).A.10%、100g B.10g C.15%、150g D.9g
(4)通过对三个方案中的碳酸钙质量分数的计算可知,方案Ⅲ计算得出的碳酸钙质量分数要比方案工和方案Ⅱ低,你认为其中可能的原因是下面的
AB
AB
(填序号).A.生成的二氧化碳有部分溶于水 B.导管中仍有部分二氧化碳未排出.
C.生成的沉淀不应该洗涤和干燥 D.稀盐酸不应加足量
(5)请你另外设计一个实验方案,测定石灰石中碳酸钙的质量分数.(提示:可以从求杂质的角度来分析)
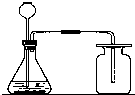 某同学利用如图所示的装置图制取二氧化碳,回答下列问题:
某同学利用如图所示的装置图制取二氧化碳,回答下列问题: