摘要: 如下图所示.烧杯内盛有一定量的稀硫酸.闭合开关后往烧杯内逐滴加入溶液直至过量.在整个过程中: (1)灯L的亮度变化情况是: (2)灵敏弹簧秤的读数变化情况是:
网址:http://m.1010jiajiao.com/timu3_id_94838[举报]
如下图所示,在20℃时,向盛有100g水的两个烧杯中分别加入20g甲、乙两种固体物质,振荡,使其充分溶解,观察到如图1所示的现象。
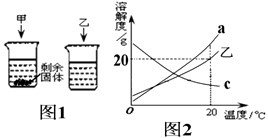
(1)20℃时,乙物质的溶解度为_________g。
(2)图1中得到的乙溶液_______(填“一定”或“不一定”)是饱和溶液。
(3)分析图1中的现象,图2中符合甲物质的溶解度曲线的是_______(填“a”或“c”)。
(4)若将图1中两烧杯内的溶液都升高温度(水分不蒸发),其溶质质量分数发生变化的是________(填“甲”或“乙”)。
查看习题详情和答案>>
(2)图1中得到的乙溶液_______(填“一定”或“不一定”)是饱和溶液。
(3)分析图1中的现象,图2中符合甲物质的溶解度曲线的是_______(填“a”或“c”)。
(4)若将图1中两烧杯内的溶液都升高温度(水分不蒸发),其溶质质量分数发生变化的是________(填“甲”或“乙”)。
如下图所示,在一个具有刻度和可以左右滑动的活塞的玻璃容器里放入白磷(足量),活塞左端管内密封有空气,右端的管口跟空气连通.将玻璃容器固定在盛有80℃热水(恒温)的烧杯上,进行实验.试回答:
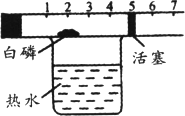
(1)实验过程中可观察到的现象是________.
(2)由此实验可以得出的结论是__________.
如图所示,某校老师为同学们准备了三套实验装置.
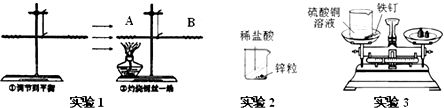
【活动目的】探究化学反应前后,反应物与生成物之间的质量关系
【查阅资料】化学反应都遵循质量守恒定律,反应前后各物质的质量总和相等.
【活动内容】实验1:在特制、耐高温、不导热的细棒两端系上细铜丝,调节到平衡,灼烧左端铜丝一段时间后,观察到细棒 端向下倾斜.
实验2:如图所示,将盛有稀盐酸(HCl)的小试管放入装有锌粒的烧杯中,称量,然后使盐酸与锌粒接触,即刻发生了化学反应生成氯化锌和氢气,化学方程式为: ,充分反应后称量.
实验3:如图称量后,将烧杯外的铁钉放入装有硫酸铜溶液的烧杯中,观察到的明显现象 ,充分反应后再次称量.
【实验总结】题(2)(3)用数字填空
(1)从表面上看,化学反应后的质量,有的减少了,有的增加了.
(2)从宏观上看,实验 正确反映了反应物与生成物之间的质量关系.
(3)从本质上看,实验 遵循质量守恒定律.
(4)由此得出结论,用实验研究化学反应前后,反应物与生成物之间的质量关系,较为科学的方法是在 体系中进行.
(5)解释实验1质量发生变化的原因 .
查看习题详情和答案>>

【活动目的】探究化学反应前后,反应物与生成物之间的质量关系
【查阅资料】化学反应都遵循质量守恒定律,反应前后各物质的质量总和相等.
【活动内容】实验1:在特制、耐高温、不导热的细棒两端系上细铜丝,调节到平衡,灼烧左端铜丝一段时间后,观察到细棒
实验2:如图所示,将盛有稀盐酸(HCl)的小试管放入装有锌粒的烧杯中,称量,然后使盐酸与锌粒接触,即刻发生了化学反应生成氯化锌和氢气,化学方程式为:
实验3:如图称量后,将烧杯外的铁钉放入装有硫酸铜溶液的烧杯中,观察到的明显现象
【实验总结】题(2)(3)用数字填空
(1)从表面上看,化学反应后的质量,有的减少了,有的增加了.
(2)从宏观上看,实验
(3)从本质上看,实验
(4)由此得出结论,用实验研究化学反应前后,反应物与生成物之间的质量关系,较为科学的方法是在
(5)解释实验1质量发生变化的原因
将盛有一定质量稀盐酸的烧杯放在天平上,然后把过量的碳酸钠加入到盛有稀盐酸的烧杯中.已知反应前烧杯内稀盐酸和碳酸钠的总质量为92.0g,从反应开始至以后的8分钟内,每1分钟读1次数并记录.结果如下:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 92.0 | 91.0 | 90.5 | 90.2 | 90.1 | 90.4 | 90.1 | 90.1 | 90.1 |
(1)烧杯内物质的质量减少的原因是______.
(2)表中有一个测定结果误差较大,这点所在的时间是第______min.
(3)在给出的坐标纸上,画出表示反应过程的质量与时间的曲线图(Ⅰ).
如果改用更浓的但HCl质量不变的盐酸重复实验(注意:假设其它条件不变,反应前烧杯内稀盐酸和碳酸钠的总质量仍为92.0g,碳酸钠过量),试在坐标纸上画出表示反应过程的质量与时间的大致曲线图(Ⅱ). 查看习题详情和答案>>
将盛有一定质量稀盐酸的烧杯放在天平上,然后把过量的碳酸钠加入到盛有稀盐酸的烧杯中.已知反应前烧杯内稀盐酸和碳酸钠的总质量为92.0g,从反应开始至以后的8分钟内,每1分钟读1次数并记录.结果如下:
试回答下列问题:
(1)烧杯内物质的质量减少的原因是______.
(2)表中有一个测定结果误差较大,这点所在的时间是第______min.
(3)在给出的坐标纸上,画出表示反应过程的质量与时间的曲线图(Ⅰ).
如果改用更浓的但HCl质量不变的盐酸重复实验(注意:假设其它条件不变,反应前烧杯内稀盐酸和碳酸钠的总质量仍为92.0g,碳酸钠过量),试在坐标纸上画出表示反应过程的质量与时间的大致曲线图(Ⅱ).
查看习题详情和答案>>
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 92.0 | 91.0 | 90.5 | 90.2 | 90.1 | 90.4 | 90.1 | 90.1 | 90.1 |
(1)烧杯内物质的质量减少的原因是______.
(2)表中有一个测定结果误差较大,这点所在的时间是第______min.
(3)在给出的坐标纸上,画出表示反应过程的质量与时间的曲线图(Ⅰ).
如果改用更浓的但HCl质量不变的盐酸重复实验(注意:假设其它条件不变,反应前烧杯内稀盐酸和碳酸钠的总质量仍为92.0g,碳酸钠过量),试在坐标纸上画出表示反应过程的质量与时间的大致曲线图(Ⅱ).