摘要:9.炼铁和炼钢的过程中有“淬火 和“回火 两种工艺.淬火是将钢铁放在火焰上烧至红热.立即放入冷水中.目的是通过消耗铁.而提高含碳量,回火是将淬火后的钢铁制品放在火焰上微热片刻后.放在空气中自然冷却.将其中的含碳量降低.使其变软.以增加韧性.试写出两步反应的化学方程式: . ,其中回火的过程中不能将制品烧至红热.主要是利用碳的化学性质 .
网址:http://m.1010jiajiao.com/timu3_id_94546[举报]
 3、请你比较一下两个“守恒定律”的表述和应用,完成下面的填空和计算:
3、请你比较一下两个“守恒定律”的表述和应用,完成下面的填空和计算:(1)参加化学反应的各物质的质量总和,
等于
反应后生成的各物质的质量总和.这个规律就叫做质量守恒定律.根据质量守恒定律,写化学反应方程式时,“等号”两边各原子的数目必须相等
.(2)能量既不会消灭,也不会创生,它只会从一种形式转化为其他形式,或者从一个物体转移到另一个物体,而在转化和转移的过程中,
能量的总和
保持不变.这个规律叫做能量守恒定律.(3)计算:根据能量守恒定律,如果图中的那个小孩开始滑下时具有1400J机械能,而滑到中点时他只剩下1150J机械能,那么滑到滑梯底端时他的动能为多少(计算时设他受到的摩擦力大小不变)?整个过程有多少机械能转化为热能?
(2012?淮安模拟)通过海水晾晒可得粗盐.粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如下图所示.

[MgCl2+2NaOH=Mg(OH)2↓+2NaCl CaCl2+Na2CO3=CaCO3↓+2NaCl]
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是
(2)操作Ⅰ和操作Ⅱ的名称是

(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,可采取用
A玻璃棒不断搅拌 B 来回移动酒精灯加热 C 来回移动蒸发皿加热
(4)在实验过程中加入过量的NaOH溶液,其实验目的是
(5)判断加入的盐酸“适量”的方法是
(6)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
查看习题详情和答案>>

[MgCl2+2NaOH=Mg(OH)2↓+2NaCl CaCl2+Na2CO3=CaCO3↓+2NaCl]
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是
水
水
.(2)操作Ⅰ和操作Ⅱ的名称是
过滤
过滤
.该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D
D
(填序号).
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,可采取用
ABC
ABC
等措施.A玻璃棒不断搅拌 B 来回移动酒精灯加热 C 来回移动蒸发皿加热
(4)在实验过程中加入过量的NaOH溶液,其实验目的是
除尽溶液中的镁离子
除尽溶液中的镁离子
.(5)判断加入的盐酸“适量”的方法是
滴加盐酸至无气泡放出为止
滴加盐酸至无气泡放出为止
.(6)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
在粗盐提纯的过程中有氯化钠生成
在粗盐提纯的过程中有氯化钠生成
.(2013?哈尔滨模拟)“锄禾日当午,汗滴禾下土,谁知盘中餐,粒粒皆辛苦”.诗中的“锄”是由(1)
查看习题详情和答案>>
铁
铁
合金制成,“汗”中含有的物质有(2)NaCl、H20等
NaCl、H20等
,“盘中餐”中大米和蔬菜给人体提供的营养素是(3)糖(类)、维生素
糖(类)、维生素
,在种植水稻和蔬菜的过程中需要施用一定量的氮肥.氮肥的作用为(4)促进植物生长(生长茂盛,叶色浓绿)
促进植物生长(生长茂盛,叶色浓绿)
,有一种氮肥,受猛烈撞击易爆炸分解成两种空气中较多的气体和一种常见液体,其反应的化学方程式为(5)2NH4NO3
2N2↑+O2↑+4H2O
| ||
2NH4NO3
2N2↑+O2↑+4H2O
,反应前后氮元素的化合价分别为(6)
| ||
-3、+5、0
-3、+5、0
.(2013?港北区二模)通过海水晾晒可得粗盐.粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如下图所示.

根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是
(2)操作Ⅰ和操作Ⅱ的过滤操作中,需要将圆形滤纸折叠处理,右图中不该出现的情形是
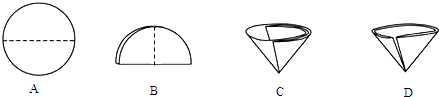
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取
(4)在实验过程中加入过量的NaOH溶液,其实验目的是
(5)判断加入的盐酸“适量”的方法是
(6)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
查看习题详情和答案>>

根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是
水)
水)
.(2)操作Ⅰ和操作Ⅱ的过滤操作中,需要将圆形滤纸折叠处理,右图中不该出现的情形是
D
D
(填序号).
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取
来回移动酒精灯加热
来回移动酒精灯加热
等措施.(4)在实验过程中加入过量的NaOH溶液,其实验目的是
除尽溶液中的镁离子
除尽溶液中的镁离子
.(5)判断加入的盐酸“适量”的方法是
滴加盐酸至无气泡放出为止
滴加盐酸至无气泡放出为止
.(6)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
提纯的过程中有氯化钠生成
提纯的过程中有氯化钠生成
.(1)实验操作必须按一定的规范进行,否则易造成实验的失败,甚至会造成事故.下列实验操作中你认为符合规范的有
A.实验桌上,易燃、易爆药品与有强氧化性的物质要分开放置并远离火源.
B.实验过程中剩余的废酸、废碱溶液应倒入水池中.
C.使用浓酸、浓碱要特别注意安全.可以用稀酸、稀碱,就不用浓酸、浓碱.
D.如果浓硫酸不慎沾到皮肤上,要立即用较多的水冲洗.
E.试管内壁被油脂玷污,先加入热的纯碱溶液洗涤,再用水冲洗
F.为证明二氧化碳已经集满,用燃着的木条伸入集气瓶中,观察火焰熄灭与否
(2)量取和稀释的过程中需要的仪器有:滴管、 、 、
(3)需要用溶质质量分数98%的浓硫酸(密度:1.84g/mL)稀释成10%的稀硫酸(密度:1.07g/mL)1000mL.计算需要浓硫酸多少毫升,水多少毫升?
查看习题详情和答案>>
A.实验桌上,易燃、易爆药品与有强氧化性的物质要分开放置并远离火源.
B.实验过程中剩余的废酸、废碱溶液应倒入水池中.
C.使用浓酸、浓碱要特别注意安全.可以用稀酸、稀碱,就不用浓酸、浓碱.
D.如果浓硫酸不慎沾到皮肤上,要立即用较多的水冲洗.
E.试管内壁被油脂玷污,先加入热的纯碱溶液洗涤,再用水冲洗
F.为证明二氧化碳已经集满,用燃着的木条伸入集气瓶中,观察火焰熄灭与否
(2)量取和稀释的过程中需要的仪器有:滴管、
(3)需要用溶质质量分数98%的浓硫酸(密度:1.84g/mL)稀释成10%的稀硫酸(密度:1.07g/mL)1000mL.计算需要浓硫酸多少毫升,水多少毫升?