摘要:11.nH2O与mH2SO4的质量比是 A.9n∶49m B.n∶m 11.A C.17n∶96m D.
网址:http://m.1010jiajiao.com/timu3_id_90282[举报]
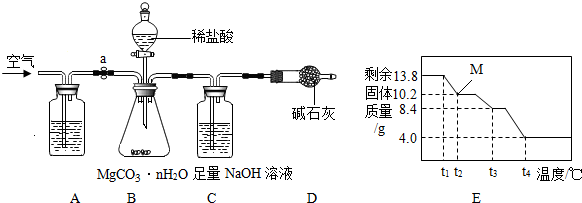
(2013?润州区二模)碳酸镁晶须(MgCO3?nH2O,n=1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域.为测定碳酸镁晶须中n的值,学习小组设计了如下装置并进行了3次实验:(不考虑稀盐酸挥发)
【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]
【实验步骤】
①
②准确称取3.45g MgCO3?nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a,
⑥准确称量C装置的质量(如上表);
⑦重复上述步骤;
⑧根据数据进行计算.
【实验分析及数据处理】
(1)A装置中盛放的溶液是
(2)D装置的作用是
(3)计算碳酸镁晶须中的n值:(要有计算过程)
【实验反思】
(4)实验结果与理论值有偏差,可以在B、C增加一个
(5)下列选项中,会造成实验结果偏大的是
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
(6)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3?nH2O进行热重分析,并绘制出图E所示的热重曲线示意图.则:
①t2℃时,剩余固体为
②最终剩余的4.0g物质是
③MgCO3?nH2O完全分解的化学方程式为:
查看习题详情和答案>>

【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]
【实验步骤】
①
检查气密性
检查气密性
;②准确称取3.45g MgCO3?nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a,
缓缓鼓入空气
缓缓鼓入空气
;| 编 号 | 1 | 2 | 3 |
| 实验前 | 228.00 | 228.00 | 228.00 |
| 实验后 | 229.10 | 229.11 | 229.09 |
⑦重复上述步骤;
⑧根据数据进行计算.
【实验分析及数据处理】
(1)A装置中盛放的溶液是
NaOH(浓)溶液
NaOH(浓)溶液
,其目的是吸收鼓入空气中的二氧化碳
吸收鼓入空气中的二氧化碳
(2)D装置的作用是
防止空气中的CO2进入C装置,造成误差
防止空气中的CO2进入C装置,造成误差
;(3)计算碳酸镁晶须中的n值:(要有计算过程)
【实验反思】
(4)实验结果与理论值有偏差,可以在B、C增加一个
除去氯化氢气体的
除去氯化氢气体的
装置以减少误差;(5)下列选项中,会造成实验结果偏大的是
②③④
②③④
;偏小的是①
①
;①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
(6)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3?nH2O进行热重分析,并绘制出图E所示的热重曲线示意图.则:
①t2℃时,剩余固体为
MgCO3和MgO
MgCO3和MgO
(填化学式);②最终剩余的4.0g物质是
MgO
MgO
(填化学式);③MgCO3?nH2O完全分解的化学方程式为:
MgCO3?nH2O
MgO+H2O+CO2↑
| ||
MgCO3?nH2O
MgO+H2O+CO2↑
.
| ||
“酒驾”是当前的热门话题之一,交警查驾驶员是否饮酒的仪器里有K2Cr2O7,该物质中Cr的化合价为 ;铁在潮湿的空气中容易生锈,为了防止铁生锈,你能采用的一种方法是 ;化学反应方程式为:aC2H6+bO2═mCO2+nH2O,则化学计量数m与n的关系为:m n(填“>”“<”或“=’).
查看习题详情和答案>>
结晶水合物X的化学式为MA2?nH2O,式中M为核电荷数不超过20的金属元素.取X 2.O3g与足量的SOCl2(亚硫酰氯)作用,SOCl2能与X的结晶水强烈反应,反应式为:SOCl2+H2O═SO2+2HCl↑.气态产物带出来的少量SOCl2要用冷冻法除去.剩余气体导入硝酸银溶液中完全反应,得到17.2g沉淀.另取X 0.609g溶于水,与硝酸银反应,得到0.860g沉淀,其中含银的质量分数为75.2%,试通过计算导出结晶水合物的化学式.
查看习题详情和答案>>
人的胃液是一种呈酸性(含盐酸)的液体,pH为0.9~1.5,试回答下列问题:
(1)正常血液的pH为7.35~7.45,与胃液相比,其要低几百万倍,已知质量分数为0.37%的盐酸的pH约为1,质量分数为0.37‰的盐酸的pH约为2,那么下列的哪种说法是正确的
A、胃液中含盐酸的质量分数明显小于0.37% B、胃液与血液都呈酸性
C、pH与溶液的H+离子浓度之间呈现正比例关系 D、人体的血液呈弱碱性
(2)胃液酸度增加就会患胃酸过多症,治疗药物的有效成分不可能是
A、NaHCO3 B、Al(OH)3 C、Ba(OH)2 D、CaCO3
(3)三硅酸镁晶体,是一种用来治疗胃溃疡的药物的主要成分,服用后能中和胃酸,作用持久.把三硅酸镁(Mg2Si3O8nH2O)改写成氧化物形式
查看习题详情和答案>>
(1)正常血液的pH为7.35~7.45,与胃液相比,其要低几百万倍,已知质量分数为0.37%的盐酸的pH约为1,质量分数为0.37‰的盐酸的pH约为2,那么下列的哪种说法是正确的
D
D
A、胃液中含盐酸的质量分数明显小于0.37% B、胃液与血液都呈酸性
C、pH与溶液的H+离子浓度之间呈现正比例关系 D、人体的血液呈弱碱性
(2)胃液酸度增加就会患胃酸过多症,治疗药物的有效成分不可能是
C
C
A、NaHCO3 B、Al(OH)3 C、Ba(OH)2 D、CaCO3
(3)三硅酸镁晶体,是一种用来治疗胃溃疡的药物的主要成分,服用后能中和胃酸,作用持久.把三硅酸镁(Mg2Si3O8nH2O)改写成氧化物形式
2MgO?3SiO2?nH2O
2MgO?3SiO2?nH2O
;写出三硅酸镁晶体中和胃酸反应的化学方程式2MgO?3SiO2?nH2O+4HCl=2MgCl2+3SiO2+(n+2)H2O
2MgO?3SiO2?nH2O+4HCl=2MgCl2+3SiO2+(n+2)H2O
.