摘要:2.解:设需要赤铁矿石的质量为x Fe2O3 + 3H2 2Fe + 3H2O 160 112 x×80 100吨 ×98% 答:略
网址:http://m.1010jiajiao.com/timu3_id_89716[举报]
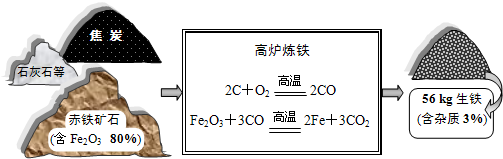
(2005?济南)请你利用图中所提供的3个数据,自拟一道有关化学方程式的计算题,并写出解答过程.
自拟试题内容部分
自拟试题解答部分
查看习题详情和答案>>

自拟试题内容部分
要制得56 kg 含杂质3%的生铁需要含Fe2O3 80%的赤铁矿石多少千克?
要制得56 kg 含杂质3%的生铁需要含Fe2O3 80%的赤铁矿石多少千克?
;自拟试题解答部分
解:设需要含Fe2O3 80%的赤铁矿石的质量为x
Fe2O3+3CO
2Fe+3CO2
160 112
x×80% 56 kg×(1-3%)
=
x=97 kg
答:要制得56 kg 含杂质3%的生铁需要含Fe2O3 80%的赤铁矿石97千克
Fe2O3+3CO
| ||
160 112
x×80% 56 kg×(1-3%)
| 160 |
| 112 |
| x×80% |
| 56kg×(1-3%) |
x=97 kg
答:要制得56 kg 含杂质3%的生铁需要含Fe2O3 80%的赤铁矿石97千克
解:设需要含Fe2O3 80%的赤铁矿石的质量为x
Fe2O3+3CO
2Fe+3CO2
160 112
x×80% 56 kg×(1-3%)
=
x=97 kg
答:要制得56 kg 含杂质3%的生铁需要含Fe2O3 80%的赤铁矿石97千克
.Fe2O3+3CO
| ||
160 112
x×80% 56 kg×(1-3%)
| 160 |
| 112 |
| x×80% |
| 56kg×(1-3%) |
x=97 kg
答:要制得56 kg 含杂质3%的生铁需要含Fe2O3 80%的赤铁矿石97千克
 (2012?哈尔滨一模)张南同学想测定某赤铁矿样品中氧化铁的质量分数,做法如下.请回答下列问题(假设赤铁矿样品中杂质不与酸反应,也不溶于水).
(2012?哈尔滨一模)张南同学想测定某赤铁矿样品中氧化铁的质量分数,做法如下.请回答下列问题(假设赤铁矿样品中杂质不与酸反应,也不溶于水).(1)配制稀盐酸,配制400g7.3%的稀盐酸.需要如图标签上标注的浓盐酸的质量是
80g
80g
;(2)将赤铁矿粉末与稀盐酸混合,反应的化学方程式是
Fe2O3+6HCl=2FeCl3+3H2O;
Fe2O3+6HCl=2FeCl3+3H2O;
;(3)取20g的赤铁矿粉与300g的7.3%的稀盐酸恰好完全反应,求解生成氯化铁质量X的比例式为
| 219 |
| 325 |
| 21.9g |
| x |
| 219 |
| 325 |
| 21.9g |
| x |
(4)此赤铁矿中氧化铁的质量分数为
80%
80%
;(5)向反应后所得溶液中加入9g水,则最终所得溶液中溶质的质量分数是
10%
10%
;(6)若用上述赤铁矿冶炼生铁63t,生铁中杂质含量为4%,炼铁过程中生铁的损失率为20%,求解需要此矿石的质量为:
120t
120t
.