摘要:一氧化碳还原氧化铜2.用赤铁矿炼铁3.甲烷在空气中燃烧4.酒精在空气中燃烧5.葡萄糖在酶的作用下氧化成水和二氧化碳 附其它常见的化学方程式
网址:http://m.1010jiajiao.com/timu3_id_8919[举报]
化学与人类的生活、生产密切相关。
请你利用所学的知识回答以下问题:
(1)钢铁工业的基本生产流程示意图如下:
请你利用所学的知识回答以下问题:
(1)钢铁工业的基本生产流程示意图如下:

①写出以赤铁矿(主要成分为Fe2O3)为原料在高温下与一氧化碳反应制取铁的化学方程式__________。
②应用化学原理分析,工业炼钢时用纯氧而不用空气的主要原因是:________________。
③铁粉与生石灰都是常用的干燥剂。现欲用化学方法检验某食品袋中的干燥剂究竟是其中的哪一种?请你简述检验方法:______________________________。
(2)氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
②应用化学原理分析,工业炼钢时用纯氧而不用空气的主要原因是:________________。
③铁粉与生石灰都是常用的干燥剂。现欲用化学方法检验某食品袋中的干燥剂究竟是其中的哪一种?请你简述检验方法:______________________________。
(2)氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:

①步骤Ⅱ中发生了两个反应,其一是2FeCl3+Fe==3FeCl2,已知所含元素化合价升高的反应是氧化反应,该物质做还原剂;反之是还原反应,该物质做氧化剂。由此判断这个反应中的氧化剂是_______(写化学式);
②步骤Ⅲ中发生反应的化学方程式是_________________;
③该流程中可以循环、回收利用的物质是:____(写化学式)。
(3)北京奥运火炬所用的燃料是丙烷(化学式为C3H8),它与甲烷(CH4)、丁烷(C4H10)、戊烷(C5H12)等属于同一系列的有机物--烷烃。根据上述几种烷烃的化学式与名称,可知:
①乙烷的化学式是____;
②含氢量最高的烷烃的化学式是____。
查看习题详情和答案>>
②步骤Ⅲ中发生反应的化学方程式是_________________;
③该流程中可以循环、回收利用的物质是:____(写化学式)。
(3)北京奥运火炬所用的燃料是丙烷(化学式为C3H8),它与甲烷(CH4)、丁烷(C4H10)、戊烷(C5H12)等属于同一系列的有机物--烷烃。根据上述几种烷烃的化学式与名称,可知:
①乙烷的化学式是____;
②含氢量最高的烷烃的化学式是____。
写出下列反应的化学方程式:
(1)木炭在氧气中充分燃烧生成二氧化碳________;
(2)在加热条件下氢气和氧化铜反应生成铜和水________;
(3)稀硫酸和硝酸钡溶液反应________.
(4)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为________.
(5)金属镁着火不能用CO2灭火,请用化学方程式表示其原因________,反应基本类型是________.
(6)用“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为:________.
”表示氧原子,则如图所示的化学反应方程式为:________.
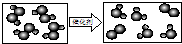
(7)写出用CaCO3、H2O、Na2CO3为原料制取NaOH的各步反应的方程式:
第一步:分解反应________;
第二步:化合反应________;
第三步:复分解反应________.
查看习题详情和答案>>
写出下列反应的化学方程式:
(1)木炭在氧气中充分燃烧生成二氧化碳 ;
(2)在加热条件下氢气和氧化铜反应生成铜和水 ;
(3)稀硫酸和硝酸钡溶液反应 .
(4)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为 .
(5)金属镁着火不能用CO2灭火,请用化学方程式表示其原因 ,反应基本类型是 .
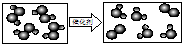
(6)用“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为: .
”表示氧原子,则如图所示的化学反应方程式为: .
(7)写出用CaCO3、H2O、Na2CO3为原料制取NaOH的各步反应的方程式:
第一步:分解反应 ;
第二步:化合反应 ;
第三步:复分解反应 . 查看习题详情和答案>>
(1)木炭在氧气中充分燃烧生成二氧化碳 ;
(2)在加热条件下氢气和氧化铜反应生成铜和水 ;
(3)稀硫酸和硝酸钡溶液反应 .
(4)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为 .
(5)金属镁着火不能用CO2灭火,请用化学方程式表示其原因 ,反应基本类型是 .
(6)用“
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为: .
”表示氧原子,则如图所示的化学反应方程式为: .
(7)写出用CaCO3、H2O、Na2CO3为原料制取NaOH的各步反应的方程式:
第一步:分解反应 ;
第二步:化合反应 ;
第三步:复分解反应 . 查看习题详情和答案>>
(1)陶、铜、铁等材料的生产离不开火,火即所谓的燃烧其实质是一种
(2)在生产和生活中大量使用的不是纯金属,而是它们的合金,合金与纯金属比较其优越的性能有(答二条)
(3)铜钱在历史上曾经是一种广泛流通的货币,已知铜的熔点是1083.4℃,铁的熔点是1534.8℃,从物理化学两个角度分析用铜铸造货币的原因:①
(4)人们的生活离不开金属,高科技材料的开发和应用也需要金属,地壳中含量最高的金属元素是
查看习题详情和答案>>
氧化反应
氧化反应
(填反应类型),而铜和铁的冶炼则主要是利用还原反应
还原反应
(填反应类型),以赤铁矿为原料写出炼铁的反应原理(用反应方程式表示)3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
在这一反应中
| ||
一氧化碳
一氧化碳
是还原剂,钢铁与氧气、水
氧气、水
直接接触容易生锈造成损失,在钢铁表面涂油漆
涂油漆
等,都能防止钢铁生锈,防止钢铁的锈蚀有利于节约金属资源
节约金属资源
、保护环境
保护环境
,提高金属的利用率.(2)在生产和生活中大量使用的不是纯金属,而是它们的合金,合金与纯金属比较其优越的性能有(答二条)
强度高
强度高
、抗腐蚀性能好
抗腐蚀性能好
,这是因为在金属中熔合了其他的金属或非金属后不仅组成
组成
发生了改变,其结构
结构
也发生了改变,从而引起性质的改变,这一事例说明了一个重要的原理是物质的组成结构决定了物质的性质
组成结构决定了物质的性质
.(3)铜钱在历史上曾经是一种广泛流通的货币,已知铜的熔点是1083.4℃,铁的熔点是1534.8℃,从物理化学两个角度分析用铜铸造货币的原因:①
铜的熔点低易铸造
铜的熔点低易铸造
②铜的抗腐蚀性能好
铜的抗腐蚀性能好
(4)人们的生活离不开金属,高科技材料的开发和应用也需要金属,地壳中含量最高的金属元素是
铝
铝
,其含量远多于铜,但铜是人类最早冶炼的金属,根据金属的性质你认为关键原因的是铜的金属活动性较弱
铜的金属活动性较弱
.莱芜素有“绿色钢城”之美誉,作为全国“钢铁十强企业”的莱钢集团为上海世博会各展馆的建设提供了数万吨钢铁材料.

(1)莱钢炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如图所示.其中焦炭的作用是
(2)高炉炼铁得到的主要产品是
A.纯铁 B.生铁 C.钢;
(3)电化学腐蚀是金属腐蚀的主要原因.当两种活泼性不同的金属在潮湿的环境中接触时,因形成原电池,活泼性强的金属首先被腐蚀.利用这一原理,为了保护轮船的钢质外壳,通常在行驶的轮船外壳上连接
(4)为了满足某些尖端技术发展的需要,人们又合成了许多新型合金材料.储氢合金是一类能够大量吸收H2,并与H2结合成金属氢化物的材料.此过程发生了
查看习题详情和答案>>

(1)莱钢炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如图所示.其中焦炭的作用是
燃烧放出热量,提供能量;与二氧化碳反应生成一氧化碳,提供还原剂
燃烧放出热量,提供能量;与二氧化碳反应生成一氧化碳,提供还原剂
.(2)高炉炼铁得到的主要产品是
B
B
,(填序号) A.纯铁 B.生铁 C.钢;
(3)电化学腐蚀是金属腐蚀的主要原因.当两种活泼性不同的金属在潮湿的环境中接触时,因形成原电池,活泼性强的金属首先被腐蚀.利用这一原理,为了保护轮船的钢质外壳,通常在行驶的轮船外壳上连接
锌
锌
(填“铜板”、“锌板”).(4)为了满足某些尖端技术发展的需要,人们又合成了许多新型合金材料.储氢合金是一类能够大量吸收H2,并与H2结合成金属氢化物的材料.此过程发生了
化学
化学
变化(填“物理”、“化学”),储氢合金属于混合物
混合物
(填“纯净物”、“混合物”).