摘要:生石灰溶于水:CaO + H2O === Ca(OH)2
网址:http://m.1010jiajiao.com/timu3_id_8855[举报]
(2012?鄂尔多斯)生石灰(CaO)在生活中常用作干燥剂,某化学研究性学习小组的同学对一包久置的生石灰干燥剂的成分产生了兴趣,进行了以下探究活动:
提出问题:这包干燥剂久置后是否变质?成分是什么?
猜想与假设:
实验探究:
(1)取部分干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂含有
(3)为了进一步确定这包干燥剂中是否还含有其他成分,小组同学设计了以下实验方案:另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中,并进行以下实验:
实验结论:通过以上实验探究得出,猜想
拓展迁移:小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意
查看习题详情和答案>>
提出问题:这包干燥剂久置后是否变质?成分是什么?
猜想与假设:
| 猜想 | 一 | 二 | 三 | 四 | 五 |
| 成分 | CaO | CaO、Ca(OH)2 | Ca(OH)2 | Ca(OH)2、CaCO3 | CaCO3 |
(1)取部分干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含
CaO
CaO
.(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂含有
CaCO3
CaCO3
.(3)为了进一步确定这包干燥剂中是否还含有其他成分,小组同学设计了以下实验方案:另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中,并进行以下实验:
| 实验方案 | 一 | 二 | 三 |
| 实验操作 | 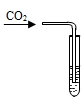 |
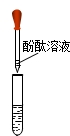 |
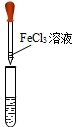 |
| 实验现象 | 澄清溶液变浑浊 | 溶液由无色变为红色 | 产生红褐色沉淀 |
| 化学方程式 | Ca(OH)2+CO2═CaCO3↓+H2O Ca(OH)2+CO2═CaCO3↓+H2O |
3Ca(OH)2+2FeCl3═3CaCl2+2Fe(OH)3↓ 3Ca(OH)2+2FeCl3═3CaCl2+2Fe(OH)3↓ |
四
四
成立.拓展迁移:小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意
密封保存
密封保存
.从锌粒、苛性钠、生石灰、食盐、纯碱、干冰六种固体物质中选出三种物质分别加入到水和稀盐酸中,产生的现象如表所示:
(1)由以上实验确定:固体B是
(2)写出化学方程式:固体A与盐酸反应
(3)六种固体物质若按单质、氧化物、酸、碱、盐来进行分类,属于碱类的是
查看习题详情和答案>>
| 固体A | 固体B | 固体C | |
| 水 | 固体不溶解 | 形成白色浑浊, 并放出大量的热 |
白色固体逐渐消失, 并吸收热量,有气泡产生 |
| 稀盐酸 | 固体逐渐溶解, 有大量气泡产生 |
白色固体逐渐溶解, 无气泡产生,放出大量的热 |
白色固体逐渐消失, 有气泡产生 |
生石灰
生石灰
,固体C是干冰
干冰
;(2)写出化学方程式:固体A与盐酸反应
Zn+2HCl=ZnCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
;固体B与水反应CaO+H2O=Ca(OH)2
CaO+H2O=Ca(OH)2
.(3)六种固体物质若按单质、氧化物、酸、碱、盐来进行分类,属于碱类的是
苛性钠
苛性钠
.已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如下转化关系.请回答下列问题.X
Y
Z
(1)写出X在点燃的条件下反应生成Y的化学方程式
(2)写出Y通过灼热碳层反应生成X的化学方程式
(3)写出由Z经过一系列反应生成烧碱的化学方程式:
(4)我们知道“物质的组成与结构决定物质的性质”是重要的化学思想.气体X、Y都含有
查看习题详情和答案>>
| 点燃 |
| 灼热碳层 |
| 石灰水 |
| 稀盐酸 |
(1)写出X在点燃的条件下反应生成Y的化学方程式
2CO+O2
2CO2
| ||
2CO+O2
2CO2
;
| ||
(2)写出Y通过灼热碳层反应生成X的化学方程式
CO2+C
2CO
| ||
CO2+C
2CO
;
| ||
(3)写出由Z经过一系列反应生成烧碱的化学方程式:
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;
| ||
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
(4)我们知道“物质的组成与结构决定物质的性质”是重要的化学思想.气体X、Y都含有
碳
碳
元素和氧
氧
元素,但它们的物理性质、化学性质都不同.请举出X、Y性质不同的一个例子一氧化碳有毒而二氧化碳无毒
一氧化碳有毒而二氧化碳无毒
.工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).主要生产流程如下:(已知2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O)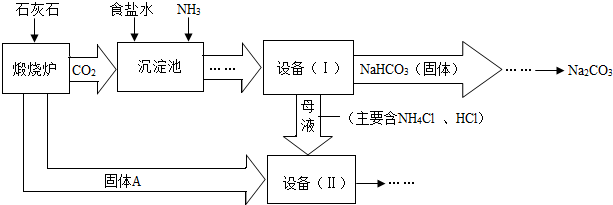
(1)“煅烧炉”中发生反应的化学方程式是
(2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是
(3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是
(4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有
(5)请写出纯碱(Na2CO3)的一点用途:
查看习题详情和答案>>

(1)“煅烧炉”中发生反应的化学方程式是
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
.
| ||
(2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是
过滤
过滤
,该操作中用到的玻璃仪器有烧杯、漏斗
漏斗
和玻璃棒
玻璃棒
.(3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是
H2O+CaO=Ca(OH)2
H2O+CaO=Ca(OH)2
.(4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有
NH3、NaCl
NH3、NaCl
(填写化学式).(5)请写出纯碱(Na2CO3)的一点用途:
用于玻璃、造纸、纺织或洗涤剂的生产等
用于玻璃、造纸、纺织或洗涤剂的生产等
.实验室有一瓶存放很久的生石灰,小丽同学想了解其变质情况,设计了实验,实验过程如下:
【实验1】取少量样品于烧杯中,加入足量水,感觉到烧杯变热,充分搅拌后过滤,得到白色沉淀和滤液.
小丽同学对样品的组成提出了以下假设:
假设1是CaO和CaCO3的混合物;
假设2是CaO和Ca(OH)2的混合物;
假设3是CaO和Ca(OH)2、CaCO3的混合物:
假设4是Ca(OH)2和CaCO3的混合物.
(1)直接可以看出,其中假设
(2)为了判断其他几种假设的合理性,她继续进行实验:
【实验2】取少量沉淀放在试管中,加入稀盐酸,出现气泡,产生气体的反应的化学方程式为:
(3)为了得到最后结论,她继续进行实验:
【实验3】取少量滤液放在另一支试管中,加入无色酚酞试液,显红色,于是小丽同学得到结论:只有假设3合理,但小明同学提出,此实验仍不能得到最后结论.你赞成
查看习题详情和答案>>
【实验1】取少量样品于烧杯中,加入足量水,感觉到烧杯变热,充分搅拌后过滤,得到白色沉淀和滤液.
小丽同学对样品的组成提出了以下假设:
假设1是CaO和CaCO3的混合物;
假设2是CaO和Ca(OH)2的混合物;
假设3是CaO和Ca(OH)2、CaCO3的混合物:
假设4是Ca(OH)2和CaCO3的混合物.
(1)直接可以看出,其中假设
4
4
不合理.(2)为了判断其他几种假设的合理性,她继续进行实验:
【实验2】取少量沉淀放在试管中,加入稀盐酸,出现气泡,产生气体的反应的化学方程式为:
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
,由此可否定假设2
2
.(3)为了得到最后结论,她继续进行实验:
【实验3】取少量滤液放在另一支试管中,加入无色酚酞试液,显红色,于是小丽同学得到结论:只有假设3合理,但小明同学提出,此实验仍不能得到最后结论.你赞成
小明
小明
同学的意见,原因是CaO+H2O═Ca(OH)2,即使没有生成氢氧化钙,氧化钙与水反应也会生成氢氧化钙,使溶液呈碱性
CaO+H2O═Ca(OH)2,即使没有生成氢氧化钙,氧化钙与水反应也会生成氢氧化钙,使溶液呈碱性
.