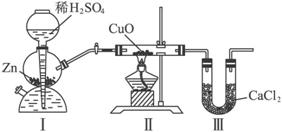
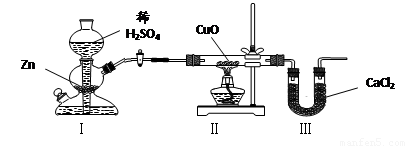
摘要:9.用下图装置测定水中氢.氧元素的质量比.其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差.实验测得m(H)∶m(O)>1∶8.下列对导致这一结果的原因的分析中.一定错误的是 ( ) A.Ⅰ.Ⅱ装置之间缺少干燥装置 B.Ⅲ装置后缺少干燥装置 C.Ⅱ装置中玻璃管内有水冷凝 D.CuO没有全部被还原 [解析] 解决此类题的关键是分析透彻此实验的反应原理:CuO+H2Cu+H2O.依据反应前后玻璃管的质量差可知生成水中氧元素的质量m(O).U形管的质量差为生成水的质量m(H2O).所以水中氢元素的质量为m(H)=m(H2O)-m(O).A项因为H2中含有水蒸气.所以m(H2O)的质量偏大.即A可能导致题中结果,B可能吸收空气中的水蒸气即m(H2O)的质量偏大.所以B可能导致题中结果,C选项相当于Ⅱ装置中玻璃管的质量反应后增加了玻璃管内冷凝的水中氢的质量.使m(O)减小.导致误差偏高,D对实验结果无影响. [答案] D
网址:http://m.1010jiajiao.com/timu3_id_87918[举报]
 用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8.下列对导致这一结果的原因的分析中,一定错误的是( )
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8.下列对导致这一结果的原因的分析中,一定错误的是( )
查看习题详情和答案>>
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是( )
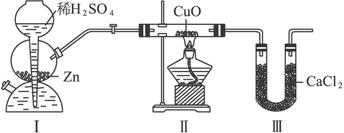
A.Ⅰ、Ⅱ装置之间缺少干燥装置 B.Ⅲ装置之后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝 D.CuO没有全部被还原
查看习题详情和答案>>
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8。下列对导致此结果的原因的分析中,一定错误的是( )

A.Ⅰ、Ⅱ装置之间缺少干燥装置 B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝 D.CuO没有全部被还原
查看习题详情和答案>>