摘要:对任意实数y.多项式的值是一个-----------[ ] A.负数 B.非负数 C.正数 D.无法确定正负
网址:http://m.1010jiajiao.com/timu3_id_8761[举报]
 碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.
碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.【探究一】碱式碳酸镁的制备
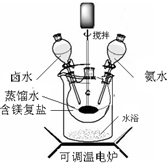
碱式碳酸镁可用复盐MgCO3?(NH4)2CO3?H2O作原料制备.取一定量的该复盐放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达 40℃时开始分解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10分钟,一段时间后过滤洗涤,滤出的固体在120℃干燥得到碱式碳酸镁产品.
回答下列问题:
(1)①搅拌的目的是
反应物充分混合接触,提高反应速率
反应物充分混合接触,提高反应速率
;②选择水浴加热方式,其优点是反应物均匀受热
反应物均匀受热
.(2)所得碱式碳酸镁产品中常检出有少量Cl-,其原因是混有
NH4Cl
NH4Cl
(填化学式).(3)设计实验检验碱式碳酸镁中含有Cl-
| 实验操作 | 实验现象 | 实验结论 |
| ①取样溶解,向样品溶液中滴加过量稀硝酸. ②再向上述所得溶液加 硝酸银或AgNO3 硝酸银或AgNO3 溶液 |
现象① 产生气泡 产生气泡 ;现象② 产生白色沉淀 产生白色沉淀 ; |
含有 Cl- |
300℃
已知:碱式碳酸镁分解反应方程式为:xMgCO3?yMg(OH)2?zH2O
| ||
探究小组利用下图测定xMgCO3?yMg(OH)2?zH2O组成.
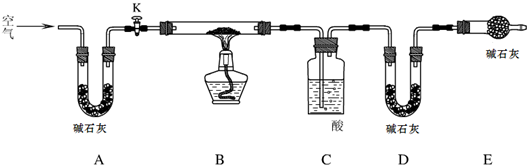
实验步骤:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:
打开活塞K,再次鼓入空气
打开活塞K,再次鼓入空气
(请补充该步操作内容).步骤5:称量相关装置的质量.
某同学在实验过程中采集了如下数据:
A.反应前玻璃管的质量100.0g
B.反应后玻璃管与残留固体总质量120.0g
C.装置C实验后增重9.0g
D.装置D实验后增重17.6g
回答下列问题:
(1)检查整套实验装置气密性的方法如下:将装置A的左端、装置E的右端分别接上导管,放入盛有水的烧杯中,
打开活塞K开关
打开活塞K开关
,对装置B用酒精灯微热,观察,若若两端导管口处均出现气泡
若两端导管口处均出现气泡
,则气密性良好;(2)如果没有装置A,则测定得到的Z值
偏大
偏大
(填“偏大”、“偏小”、“无影响”),装置C中的酸为
浓硫酸
浓硫酸
(写名称);(3)根据实验测定的数据,求出碱式碳酸铜(xMgCO3?yMg(OH)2?zH2O)
中x:y:z=
4:1:4
4:1:4
(要求写出过程).【交流反思】
(4)如果不称量装置C实验前后的增重,要根据实验数据,求出x:y:z的值,还可测量的实验数据是
样品的质量
样品的质量
.科技人员已研制出一种以甲醇为原料的新型手机电池,其容量为普通电池的10倍,该电池的化学原理可表示为xCH4O+3O2+yNaOH═2Na2CO3+zH2O,则x,y,z的值分别是( )
| A、2,4,6 | B、1,2,3 | C、2,4,7 | D、3,5,6 |
有A、B、C、D四种元素.A+最外电子层是第三层,已达到稳定结构.B3+具有与氖原子相同的电子层结构.C2-比氦原子多16个电子.D是地壳中含量最大的元素.这四种元素可形成化学式为AB(CDx)y的化合物,其电离方程式为:AB(CDx)y=A++B3++
yCDxn-在此化合物的水溶液中阴、阳离子个数比为1:1.C元素在此化合物中的化合价比硝酸的酸酐中氮元素的化合价还高1价.
(1)写出这四种元素的元素符号:A
(2)用字母A、C、D表示A、C、D三元素两两之间形成的常见化合物的化学式
(3)确定x、y、n的值(要求写出确定过程),并写出AB(CDx)y所代表的物质的化学式
查看习题详情和答案>>
yCDxn-在此化合物的水溶液中阴、阳离子个数比为1:1.C元素在此化合物中的化合价比硝酸的酸酐中氮元素的化合价还高1价.
(1)写出这四种元素的元素符号:A
K
K
,BAl
Al
,CS
S
,DO
O
.(2)用字母A、C、D表示A、C、D三元素两两之间形成的常见化合物的化学式
K2S、K2O、SO2、SO3
K2S、K2O、SO2、SO3
.(3)确定x、y、n的值(要求写出确定过程),并写出AB(CDx)y所代表的物质的化学式
KAl(SO4)2
KAl(SO4)2
.