网址:http://m.1010jiajiao.com/timu3_id_86830[举报]
(1)制备实验开始时,先检查装置气密性,接下来的操作依次是______(填序号)
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加人浓盐酸
(2)制备反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量.
乙方案:采用酸碱中和滴定法测定.
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量.
丁方案:与足量Zn 反应,测量生成的H2体积.
继而进行下列判断和实验:
①判定甲方案不可行,理由是______.
②进行乙方案实验:准确量取残余清液稀释一定倍数后作为试样.
a.量取试样20.00mL,用0.1000mol?L-1 NaOH标准溶液滴定,消耗22.00mL,该次滴定测得试样中盐酸浓度为______mol?L-1
b.平行滴定后获得实验结果.
③判断丙方案的实验结果______(填“偏大”、“偏小”或“准确”).
[已知:Ksp(CaCO3 )=2.8×10-9、Ksp(MnCO3 )=2.3×10-11
④进行丁方案实验:装置如右图2所示(夹持器具已略去).
(i) 使Y形管中的残余清液与锌粒反应的正确操作是将______转移到______中.
(ii)反应完毕,每间隔1 分钟读取气体体积,气体体积逐次减小,直至不变.气体体积逐次减小的原因是______(排除仪器和实验操作的影响因素).
 查看习题详情和答案>>
查看习题详情和答案>>
实验室常利用甲醛法测定
(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO 3H++6H2O+(CH2)6N4H+(
3H++6H2O+(CH2)6N4H+(
步骤Ⅰ
称取1.500 g样品,加水溶解,配成250 mL溶液.步骤
Ⅱ 用酸式滴定管量取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液.用0.1010 mol·L-1的NaOH标准溶液滴定至终点.按上述操作方法再重复2次.(1)根据实验步骤填空:
①步骤
Ⅰ中用到的主要玻璃仪器有________.②
下列情况使样品中氮质量分数偏低的是________.a.
步骤Ⅱ中酸式滴定管用蒸馏水洗涤后,直接加入样品溶液进行量取b.锥形瓶用蒸馏水洗涤后,水未倒尽
c.滴定时对NaOH标准溶液体积,读取初读数时仰视,读取终读数时姿势正确
d.滴定管在滴定前有气泡,滴定后气泡消失
③滴定达到终点的现象________.
(2)滴定结果如表所示:
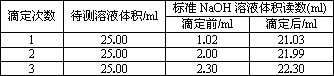
则消耗NaOH标准溶液的体积平均为________,该样品中氮的质量分数为________.
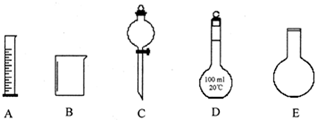
(1)上述仪器中,C的名称是
(2)实验室制备氯气的发生装置中,需用到上述仪器中的C和
(3)下列关于仪器D的使用方法中,正确的是
A.使用前应检验是否漏液
B.使用前必须烘干
C.不能用作物质反应或溶解的容器. 查看习题详情和答案>>

(1)写出仪器C、E的名称
(2)分离以下混合物应该主要选用使用什么仪器?(填字母符号)
粗盐和泥沙:
(3)下列关于仪器的使用说法正确的是
A.A仪器可以用酒精灯直接加热
B.B仪器可以用于向酒精灯中添加酒精
C.C仪器在放出液体时应打开上边的瓶塞
D.在实验室应用D仪器进行实验时要不断用玻璃棒搅拌
E.E仪器中水的流向是上进下出
(4)若向C装置中加入碘水和少量CCl4,震荡后静置,会观察到什么现象?
(5)若粗盐溶液中仅含有少量的CaCl2,某学生用Na2CO3使Ca2+离子转化为碳酸钙沉淀,确认Ca2+已沉淀完全的实验方法是
Ca2+没有沉淀完全
Ca2+没有沉淀完全
(12分)环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g-cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)* | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 |
|
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇为放热反应,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55-60℃进行反应。反应完成后,加入适量水,蒸馏,收集95-100℃的馏分,得到主要的含环己酮和水的混合物。
①酸性Na2Cr2O7溶液的加料方式为 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a蒸馏,收集151-156℃的馏分;
b 过滤;
c 在收集到的馏分中加NaCl固体至饱和,静置,分液;
d 加入无水MgSO4固体,除去有机物中少量水。
①上述操作的正确顺序是 (填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需 、 。
③在上述操作c中,加入NaCl固体的作用是 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学环境的氢原子。
查看习题详情和答案>>