网址:http://m.1010jiajiao.com/timu3_id_86581[举报]
A组 | B组 | C组 | D组 |
金刚石:3 | Li: | HF: | NaCl: |
硅晶体:1 | Na: | HCl: | KCl: |
硼晶体:2 | K: | HBI: | RbCl: |
二氧化硅:1 | Rb: | HI: | CsCl: |
据此回答下列问题:
(1)A组属于_____________晶体,其熔化时克服的微粒间的作用力是_________________;
(2)B组晶体共同的物理性质是_____________(填序号);
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于__________________________;
(4)D组晶体可能具有的性质是_____________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
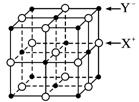
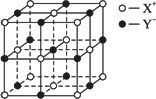
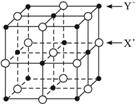
(5)XY晶体的单元结构如下图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为NA mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为__________g·mol-1。

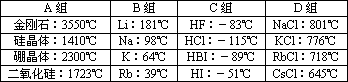
现有几组物质的熔点数据如下表:
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________;
(2)B组晶体共同的物理性质是________(填序号);
①有金属光泽 ②导电性
③导热性 ④延展性
(3)C组中HF熔点反常是由于________;
(4)D组晶体可能具有的性质是________(填序号).
①硬度小 ②水溶液能导电
③固体能导电 ④熔融状态能导电
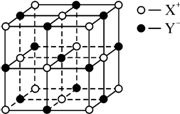
(5)XY晶体的单元结构如图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为NA mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为________g·mol-1.
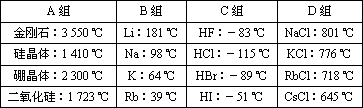
(经典回放)现有几组物质的熔点数据如下表:
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________.
(2)B组晶体共同的物理性质是________(填序号).
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于________.
(4)D组晶体可能具有的性质是________(填序号).
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)XY晶体的单元结构如图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为Na mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为________g·mol-1.
A组 | B组 | C组 | D组 |
金刚石:3550 ℃ | Li:181 ℃ | HF:-83 ℃ | NaCl:801 ℃ |
硅晶体:1410 ℃ | Na:98 ℃ | HCl:-115 ℃ | KCl:776 ℃ |
硼晶体:2300 ℃ | K:64 ℃ | HBr:-89 ℃ | RbCl:718 ℃ |
二氧化硅1723 ℃ | Rb:39 ℃ | Hi:-51 ℃ | CsCl:645 ℃ |
据此完成下列问题:
(1)A组属于__________晶体,其熔化时克服的粒子间的作用力是__________。
(2)B组晶体共同的物理性质是__________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性?
(3)C组中HF熔点反常是由于____________________。
(4)D组晶体可能具有的性质是__________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)XY晶体的单元结构如下图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为NA mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为__________g·mol-1。
查看习题详情和答案>>
现有几种物质的熔点数据如下表:
| A组 | B组 | C组 | D组 |
| 金刚石:3 550℃ | Li:181℃ | HF:-83℃ | NaCl:801℃ |
| 硅晶体:1 410℃ | Na:98℃ | HCl:-115℃ | KCl:776℃ |
| 硼晶体:2 300℃ | K:64℃ | HBr:-89℃ | RbCl:718℃ |
| 二氧化硅1 723℃ | Rb:39℃ | HI:-51℃ | CsCl:645℃ |
据此完成下列问题:
(1)A组属于_______________晶体,其熔化时克服的粒子间的作用力是_______________。
(2)B组晶体共同的物理性质是_______________ (填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于______________________________。
(4)D组晶体可能具有的性质是_______________ (填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)XY晶体的单元结构如下图所示,晶体中距离最近的X+与Y-的核间距离为a cm,已知阿伏加德罗常数为Na mol-1,其密度为ρ g·cm-3,则XY的摩尔质量可表示为________ g·mol-1。