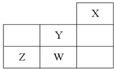
摘要:18.短周期元素W.X.Y.Z在元素周期表中的相对位置如下表所示.其中X.Y.Z三种元素的质子数之和为21. W X Y Z (1)W与Z可形成原子个数比为1?1的化合物.其电子式为 . (2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应.生成物的水溶液呈酸性.其原因是 ,该溶液中各种离子浓度由大到小的顺序为 . (3)由XW4.Z2和KOH溶液组成的新型燃料电池中.负极上发生反应的电极反应式为 . (4)已知:2YZ2(g)⇌Y2Z4(g),ΔH<0.在恒温恒容条件下.将一定量YZ2和Y2Z4的混合气体通入容积为2 L的密闭容器中.反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示. ①a.b.c.d四个点中.化学反应处于平衡状态的是 点. ②25 min时.增加了 mol. ③a.b.c.d四个点所表示的反应体系中.气体颜色由深到浅的顺序是 . 解析:X.Y.Z分别为ⅣA.ⅤA.ⅥA族元素.根据其质子数之和为21.可以推断X为C.Y为N.Z为O.进而推断W为H.(1)H和O形成的原子个数比为1:1的化合物为H2O2.其电子式为H?H.(2)N的最高价氧化物对应的水化物HNO3与其氢化物NH3恰好反应生成NH4NO3.由于NH水解.溶液显酸性.(3)CH4.O2和KOH溶液组成的燃料电池中.负极CH4发生氧化反应.电极反应式为:CH4-8e-+10OH-===CO+7H2O.(4)①图象中b.d点处于平衡状态.②根据图象.M曲线代表NO2.N曲线代表N2O4,25 min时NO2增加的物质的量为:mol/L×2 L=0.8 mol.③NO2的体积分数越大.气体颜色越深.故气体颜色由深到浅的顺序为cdba. 答案:(1)HH (2)NH+H2ONH3·H2O+H+ c(NO)>c(NH)>c(H+)>c(OH-) (3)CH4-8e-+10OH-===CO+7H2O (4)①b.d ②NO2 0.8 ③cdba
网址:http://m.1010jiajiao.com/timu3_id_85800[举报]
 短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中不正确的是( )
短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中不正确的是( )| A、X元素形成的单质中存在非极性共价键 | B、W的最高价氧化物对应的水化物是强酸 | C、Y的原子半径在同周期主族元素中最小 | D、Z的气态氢化物的稳定性在同主族元素中最强 |
短周期元素W、X、Y、Z 的原子序数依次增大,W与Y,X与Z位于同一主族.W与X可形成共价化合物WX2.Y原子的内层电子总数是其最外层电子数的2.5倍,Y的单质常作为半导体材料.下列叙述中不正确的是( )
查看习题详情和答案>>