摘要:7.有Fe2+.NO.Fe3+.NH.H+和H2O六种粒子.分别属于同一氧化还原反应中的反应物和生成物.下列叙述不正确的是( ) A.该过程中氧化剂与还原剂的物质的量之比为1?8 B.该过程说明Fe(NO3)2溶液不宜加酸酸化 C.若有1 mol NO发生氧化反应.则转移8 mol e- D.若把该反应设计为原电池.则负极反应为Fe2+-e-===Fe3+ 解析:由于酸性条件下的NO具有强氧化性.Fe2+具有还原性.则反应的方程式为:8Fe2++10H++NO===8Fe3++NH+3H2O.故A项正确,B项.正确.因为加酸酸化后.NO会将Fe2+氧化,C项.不正确.因为NO发生的是还原反应.不是氧化反应,D项.原电池的负极发生氧化反应.故正确. 答案:C
网址:http://m.1010jiajiao.com/timu3_id_85321[举报]
有Fe2+、NO 、Fe3+、NH
、Fe3+、NH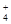 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2 溶液不宜加酸酸化
C. 若有1 mol NO 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ — e- = Fe3+
查看习题详情和答案>>
有Fe2+、NO![]() 、Fe3+、NH
、Fe3+、NH![]() 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2 溶液不宜加酸酸化
C. 若有1 mol NO![]() 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ — e- = Fe3+
查看习题详情和答案>>有Fe2+、NO![]() 、Fe3+、NH
、Fe3+、NH![]() 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2溶液不宜加酸酸化
C. 若有1 mol NO![]() 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ — e-= Fe3+
查看习题详情和答案>>
|
有Fe2+、NO | |
| [ ] | |
A. |
氧化剂与还原剂的物质的量之比为1∶8 |
B. |
该过程说明Fe(NO3)2溶液不宜加酸酸化 |
C. |
若有1 mol NO |
D. |
若把该反应设计为原电池,则负极反应为Fe2+-e- |
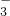 、Fe3+、NH
、Fe3+、NH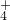 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是