摘要:常温下.VaL pH=2的盐酸与VbL pH=12的氨水混合.若所得溶液显酸性.下列有关判断正确的是( ) A.Va一定等于Vb B. Va大于或等于Vb C. 混合溶液中离子浓度一定满足:c(Cl-)>c(NH)> c(H+)>c(OH-) D. 混合溶液中离子浓度一定满足:c(NH)+c(H+)= c(Cl-)+c(OH-) 解析:两种溶液中c(H+)=c(OH-)=0.01 mol/L.故c(NH3·H2O)>c(HCl).若Va=Vb.则碱过量.反应后的溶液呈碱性,若二者恰好反应.则反应后的溶液呈酸性.此时Va>Vb,若酸过量.则反应后溶液仍为酸性,若盐酸过量很多.则反应后的溶液中c(H+)>c(NH).A.B.C错,依电荷守恒原理知D对. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_85249[举报]
下列溶液中有关物质的量浓度关系正确的是
A.将0.2 mol/L的某一元弱酸HA溶液和0.1 mol/LNaOH溶液等体积混合,则充分反应后的混合液中:2c(OH-)+c(A-)=2c(H+)+c(HA)
B.pH相等的CH3COONa溶液、C6H5ONa溶液、NaHCO3溶液和NaOH溶液,其物质的量浓度由小到大的顺序为:c (NaOH)<c(CH3COONa)<c (NaHCO3)<c (C6H5ONa)
C.常温下,将pH=2.0的CH3COOH溶液和pH=12.0的NaOH溶液等体积混合,则充分反应后的混合液中:c (Na+)>c (CH3COO-)>c(OH-)>c (H+)
D.常温下,向10mL pH=4.0的醋酸溶液中加入水稀释后,溶液中c(H+)、c(OH-)、c (CH3COOH)/c (CH3COO-)都将要变小
查看习题详情和答案>>
常温下,取pH=2的两种二元酸H2A与H2B各1 mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述正确的是 ( )
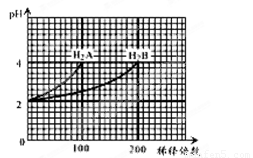
A.H2A的电离方程式为H2A===H++HA-,HA-  H++A2-
H++A2-
B.pH=4的NaHA水溶液中离子浓度大小为c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-)
C.含NaHA、NaHB的混合液离子浓度大小为c(Na+)=c(A2-)+c(HB-)+c(H2B)+c(B2-)
D.Na2B的水溶液中,离子浓度大小为c(Na+)>c(B2-)>c(OH-)>c(H+)
查看习题详情和答案>>
 MgCl2+6H2O
MgCl2+6H2O