摘要:4.下列实验设计及其对应离子方程式均正确的是( ) A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+===Cu2++2Fe2+ B.Na2O2与H2O反应制备O2:Na2O2+H2O===2Na++2OH-+O2↑ C.将氯气溶于水制备次氯酸:Cl2+H2O===2H++Cl-+ClO- D.用浓盐酸酸化的KMnO4与H2O2反应.证明H2O2具有还原性:2MnO+6H++5H2O2===2Mn2++5O2↑+8H2O 解析:B中Na2O2与水反应的离子方程式中氧原子不守恒且电子不守恒.B错误,次氯酸为弱酸.不能拆写成H+和ClO-.且Cl2与H2O的反应为可逆反应.C错误,KMnO4具有强氧化性.能将Cl-氧化成Cl2.故酸化KMnO4不能用盐酸酸化.应使用稀H2SO4.D错误. 答案:A
网址:http://m.1010jiajiao.com/timu3_id_84938[举报]
下列实验设计及其对应离子方程式均正确的是( )
查看习题详情和答案>>
A.用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO
| ||
| B.Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | ||
C.稀盐酸滴在石灰石上:CO
| ||
| D.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
下列实验设计及其对应离子方程式均正确的是( )
A.用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO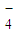 +6H++5H2O2═2Mn2++5O2↑+8H2O
+6H++5H2O2═2Mn2++5O2↑+8H2O
B.Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑
C.稀盐酸滴在石灰石上:CO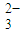 +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
D.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+
查看习题详情和答案>>
A.用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO
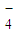 +6H++5H2O2═2Mn2++5O2↑+8H2O
+6H++5H2O2═2Mn2++5O2↑+8H2OB.Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑
C.稀盐酸滴在石灰石上:CO
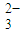 +2H+═CO2↑+H2O
+2H+═CO2↑+H2OD.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+
查看习题详情和答案>>
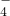 +6H++5H2O2═2Mn2++5O2↑+8H2O
+6H++5H2O2═2Mn2++5O2↑+8H2O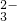 +2H+═CO2↑+H2O
+2H+═CO2↑+H2O