摘要:14.通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能.已知部分化学键的键能如下: 化学键 N-H N-N O==O NN O-H 键能 386 167 498 946 460 (1)发射神舟飞船的长征火箭用了肼(N2H4.气态)为燃料.若它在氧气中燃烧.生成N2和H2O.1 mol肼完全燃烧时放出的热量为 . (2)为了提高肼(N2H4)燃烧过程中释放的能量.常用二氧化氮作氧化剂代替氧气.这两者反应生成氮气和水蒸气.且: ①N2(g)+2O2(g)===2NO2(g),ΔH1=+67.7 kJ/mol ②N2H4(g)+O2(g)===N2(g)+2H2O(g),ΔH2=-534 kJ/mol 试写出肼和NO2完全反应的热化学方程式: . 解析:(1)根据题意.肼燃烧时发生反应为N2H4(g)+O2(g)===N2(g)+2H2O(l),故ΔH=[+498]-=-577 kJ/mol.即1 mol肼完全燃烧时放出的热量为577 kJ. (2)根据题意.要求计算下列反应的反应热:③N2H4(g)+NO2(g)===3/2N2(g)+2H2O(g),ΔH3.根据盖斯定律.一个反应的反应热的大小仅与其始态和终态有关.而与其过程无关.则存在:③=②-①÷2.即:ΔH3=ΔH2-ΔH1÷2=-567.85 kJ/mol. 答案:(1)577 kJ (2)N2H4(g)+NO2(g)===3/2N2(g)+2H2O(g),ΔH3=-567.85 kJ/mol
网址:http://m.1010jiajiao.com/timu3_id_84924[举报]
|
通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(ΔH).下面列举了一些化学键的键能数据,供计算用:
工业上高纯硅可以通过下列反应制取:SiCl4(g)+2H2(g) | |
| [ ] | |
A. |
+412 kJ/mol |
B. |
-412 kJ/mol |
C. |
+236 kJ/mol |
D. |
-236 kJ/mol |
(6分)通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能. 已知部分化学键的键能如下:
| 化学键 | N—H | N—N | O==O | N≡N | O—H |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
(2)为了提高肼(N2H4)燃烧过程中释放的能量,常用二氧化氮作氧化剂代替氧气,这两者反应生成氮气和水蒸气.且:
①N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
②N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试写出肼和NO2完全反应的热化学方程式:____________________________________
(3)随着中国空间技术的发展,中俄于2009年携手探火星工程,寻找更高效的火箭推进剂也被提到了议事日程.在实验室我国科研人员应用电子计算机模拟出具有高能量的物质N60,它的结构与C60十分相似.已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有________个N—N键. 查看习题详情和答案>>
(6分)通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能. 已知部分化学键的键能如下:
(1)发射神舟飞船的长征火箭用了肼(N2H4,气态)为燃料,若它在氧气(气态)中燃烧,生成N2(气态)和H2O(液态).1 mol肼完全燃烧时放出的热量为________ .
(2)为了提高肼(N2H4)燃烧过程中释放的能量,常用二氧化氮作氧化剂代替氧气,这两者反应生成氮气和水蒸气.且:
①N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
②N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试写出肼和NO2完全反应的热化学方程式:____________________________________
(3)随着中国空间技术的发展,中俄于2009年携手探火星工程,寻找更高效的火箭推进剂也被提到了议事日程.在实验室我国科研人员应用电子计算机模拟出具有高能量的物质N60,它的结构与C60十分相似.已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有________个N—N键.
| 化学键 | N—H | N—N | O==O | N≡N | O—H |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
(2)为了提高肼(N2H4)燃烧过程中释放的能量,常用二氧化氮作氧化剂代替氧气,这两者反应生成氮气和水蒸气.且:
①N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
②N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试写出肼和NO2完全反应的热化学方程式:____________________________________
(3)随着中国空间技术的发展,中俄于2009年携手探火星工程,寻找更高效的火箭推进剂也被提到了议事日程.在实验室我国科研人员应用电子计算机模拟出具有高能量的物质N60,它的结构与C60十分相似.已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有________个N—N键.
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”=):SiC_______Si;SiCl4_______SiO2。
(2)图1-1立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子。
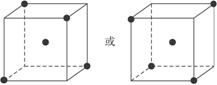
图1-1
查看习题详情和答案>>
通常人们把拆开1 mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g) ![]() Si(s)+4HCl (g)
Si(s)+4HCl (g)
该反应的反应热ΔH=______________kJ·mol -1
查看习题详情和答案>>