摘要:2.(2010·四川省绵阳市诊断性测试)玻璃棒是化学实验中常用的仪器.下列有关实验过程需要使用玻璃棒进行操作的是( ) ①用pH试纸测定溶液的pH ②将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体 ③从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl ④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验 ⑤用适量的蔗糖.浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验 ⑥实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀 A.①②⑥ B.③④⑥ C.②④⑤ D.①③⑤ 解析:①需用玻璃棒蘸取待测液来测定其pH,③分离MnO2.KCl混合物时需过滤.过滤用玻璃棒进行引流,⑤需用玻璃棒进行搅拌.使反应更充分. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_84840[举报]
玻璃棒是化学实验中常用的仪器,通常用于搅拌、引流等.下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是( )
| A、用pH试纸测定Na2CO3溶液的pH | B、从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl | C、用新制的FeSO4溶液和NaOH溶液制备Fe(OH)2 | D、用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验 |
 Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是
Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是A.用pH试纸测定Na2CO3溶液的pH
B.从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
C.实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
D.配制一定物质的量浓度的氯化钠溶液
E.取某溶液做焰色反应实验,说明该溶液中含有钠元素
F.用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
G.促使过饱和的硝酸钾溶液析出晶体
Ⅱ.二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.ClO2是一种黄绿色的气体,易溶于水.实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
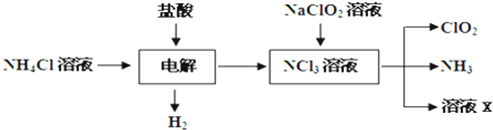
(1)写出电解时发生反应的化学方程式:
(2)除去ClO2中的NH3可选用的试剂是
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.水
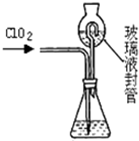
(3)测定ClO2(如右图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL足量硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收(假设吸收完全);将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定 (I2+2S2O32-=2I-+S4O62-),共用去V mL硫代硫酸钠溶液.
①装置中玻璃液封管的作用是
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式
③测得ClO2的质量m(ClO2)=
实验室配制480mL 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
(2)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
(3)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
(4)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
(5)若实验时遇到下列情况,将使溶液的浓度偏低的是
A.配制前设有将容量瓶中的水除尽;
B.试剂溶解后,在转移到容量瓶中时有洒出;
C.忘记将洗涤液转入容量瓶;
D.定容、摇匀、静置后发现凹液面低于刻度线又加水至刻度线;
E.定容时俯视刻度线.
查看习题详情和答案>>
(1)应用托盘天平称取十水碳酸钠晶体
14.3
14.3
g,应选用500
500
m L的容量瓶.(2)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
①③⑤
①③⑤
.(填数字符号)(3)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
dbac
dbac
.(填写字母,每种仪器只能选择一次)(4)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
2
2
种用途.(填写数字)(5)若实验时遇到下列情况,将使溶液的浓度偏低的是
BCD
BCD
.A.配制前设有将容量瓶中的水除尽;
B.试剂溶解后,在转移到容量瓶中时有洒出;
C.忘记将洗涤液转入容量瓶;
D.定容、摇匀、静置后发现凹液面低于刻度线又加水至刻度线;
E.定容时俯视刻度线.
玻璃棒是化学实验中常用的仪器之一,其主要用于搅拌、过滤或转移液体时的引流.下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是( )
①用pH试纸测定Na2C03溶液的pH
②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
④配制一定物质的量浓度的氯化钠溶液
⑤取某溶液做焰色反应实验,检验该溶液中是否含有钠元素
⑥用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
⑦促使过饱和的硝酸钾溶液析出晶体
⑧用倾析法分离、洗涤颗粒较大的沉淀.
①用pH试纸测定Na2C03溶液的pH
②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
④配制一定物质的量浓度的氯化钠溶液
⑤取某溶液做焰色反应实验,检验该溶液中是否含有钠元素
⑥用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
⑦促使过饱和的硝酸钾溶液析出晶体
⑧用倾析法分离、洗涤颗粒较大的沉淀.
查看习题详情和答案>>
请按要求完成下面各小题.
Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,一般不需要使用玻璃棒进行操作的是
①用pH试纸测定NaHCO3溶液的pH
②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验
⑤将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
⑥用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
⑦探究Ba(OH)2?8H2O晶体和NH4Cl晶体反应过程中的能量变化
Ⅱ.设计简单实验证明:氧化性Cl2>FeCl3>KI.简述实验步骤、现象和结论.
可供选用的试剂有:氯水、氯化铁溶液、碘水、氢氧化钠溶液、稀硫酸、硫氰化钾溶液、碘化钾淀粉溶液、氯化亚铁溶液、过氧化氢溶液、蒸馏水;仪器为中学化学实验常用仪器,自选.
Ⅲ.实验室用表面带有少量铁锈(Fe2O3?xH2O)的铁屑制取绿矾(FeSO4?7H2O).
①实验中应控制药品量的使用,应使
②制备过程中有关反应的化学方程式:
③反应结束后精制绿矾,精制过程中需将溶液加热至50℃~80℃.为减少过滤时绿矾的损失,应将溶液
查看习题详情和答案>>
Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,一般不需要使用玻璃棒进行操作的是
③④⑤
③④⑤
①用pH试纸测定NaHCO3溶液的pH
②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验
⑤将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
⑥用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
⑦探究Ba(OH)2?8H2O晶体和NH4Cl晶体反应过程中的能量变化
Ⅱ.设计简单实验证明:氧化性Cl2>FeCl3>KI.简述实验步骤、现象和结论.
可供选用的试剂有:氯水、氯化铁溶液、碘水、氢氧化钠溶液、稀硫酸、硫氰化钾溶液、碘化钾淀粉溶液、氯化亚铁溶液、过氧化氢溶液、蒸馏水;仪器为中学化学实验常用仪器,自选.
①取FeCl2溶液少许,加入KSCN溶液,无明显现象,加氯水少许,变为血红色溶液,说明氧化性Cl2>FeCl3;
②取无色的碘化钾淀粉溶液,加入FeCl3溶液,变蓝色,说明氧化性FeCl3>KI.
②取无色的碘化钾淀粉溶液,加入FeCl3溶液,变蓝色,说明氧化性FeCl3>KI.
①取FeCl2溶液少许,加入KSCN溶液,无明显现象,加氯水少许,变为血红色溶液,说明氧化性Cl2>FeCl3;
②取无色的碘化钾淀粉溶液,加入FeCl3溶液,变蓝色,说明氧化性FeCl3>KI.
②取无色的碘化钾淀粉溶液,加入FeCl3溶液,变蓝色,说明氧化性FeCl3>KI.
Ⅲ.实验室用表面带有少量铁锈(Fe2O3?xH2O)的铁屑制取绿矾(FeSO4?7H2O).
①实验中应控制药品量的使用,应使
铁屑
铁屑
(填名称)稍过量.②制备过程中有关反应的化学方程式:
Fe+H2SO4═FeSO4+H2↑、3H2SO4+Fe2O3?xH2O═Fe2(SO4)3+(3+x)H2O、Fe2(SO4)3+Fe═3FeSO4
Fe+H2SO4═FeSO4+H2↑、3H2SO4+Fe2O3?xH2O═Fe2(SO4)3+(3+x)H2O、Fe2(SO4)3+Fe═3FeSO4
③反应结束后精制绿矾,精制过程中需将溶液加热至50℃~80℃.为减少过滤时绿矾的损失,应将溶液
趁热过滤
趁热过滤
.