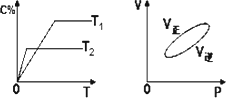
摘要:7.可逆反应aA(g)+bB(g) cC(g)+dD(s) ΔH=Q kJ/mol.反应过程中.当其他条件不变时.C在混合物中的含量与温度(T)的关系如图Ⅰ所示.反应速率(v)与压强(p)的关系如图Ⅱ所示.据图分析.以下说法正确的是( ) A.T1<T2.Q>0 B.增大压强.B的转化率减小 C.当反应达到平衡时.混合气体的密度不再变化 D.a+b>c+d 解析:A项.根据图象Ⅰ.T2时达到平衡所需时间短.故温度:T2>T1.从T1到T2.升温.C%降低.表明升高温度.平衡向逆反应方向移动.则正反应为放热反应.Q<0.故不正确,B项.由图象Ⅱ可知.增大压强.v正>v逆.平衡向正反应方向移动.则B的转化率增大.故不正确,由上述可知.a+b>c.D物质是固体.故不能确定a+b是否大于c+d.不正确. 答案:C
网址:http://m.1010jiajiao.com/timu3_id_84826[举报]
可逆反应aA(g)+bB(g) cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是

A.T1<T2,Q>0
B.增大压强,B的转化率减小
C.当反应达平衡时,混合气体的密度不再变化
D.a+b>c+d
查看习题详情和答案>>
可逆反应aA(g)+bB(g) cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是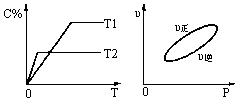
| A.T1<T2,Q>0 |
| B.增大压强,B的转化率减小 |
| C.当反应达平衡时,混合气体的密度不再变化 |
| D.a+b>c+d |
可逆反应aA(g)+bB(g) cC(g)+dD(s) ΔH=Q kJ/mol,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图Ⅰ所示,反应速率(v)与压强(p)的关系如图Ⅱ所示.据图分析,以下说法正确的是
cC(g)+dD(s) ΔH=Q kJ/mol,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图Ⅰ所示,反应速率(v)与压强(p)的关系如图Ⅱ所示.据图分析,以下说法正确的是
 cC(g)+dD(s) ΔH=Q kJ/mol,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图Ⅰ所示,反应速率(v)与压强(p)的关系如图Ⅱ所示.据图分析,以下说法正确的是
cC(g)+dD(s) ΔH=Q kJ/mol,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图Ⅰ所示,反应速率(v)与压强(p)的关系如图Ⅱ所示.据图分析,以下说法正确的是
[ ]
A.T1<T2,Q>0
B.增大压强,B的转化率减小
C.当反应达到平衡时,混合气体的密度不再变 化
D.a+b>c+d
查看习题详情和答案>>
B.增大压强,B的转化率减小
C.当反应达到平衡时,混合气体的密度不再变 化
D.a+b>c+d
可逆反应aA(g)+bB(g)![]() cC(g)+dD(s);ΔH=Q kJ/mol,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是( )
cC(g)+dD(s);ΔH=Q kJ/mol,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是( )
A.T1<T2,Q>0
B.增大压强,B的转化率减小
C.当反应达平衡时,混合气体的密度不再变化
D.a+b>c+d

|
可逆反应aA(g)+bB(g)
| |
| [ ] | |
A. |
T1<T2,Q>0 |
B. |
增大压强,B的转化率减小 |
C. |
当反应达平衡时,混合气体的密度不再变化 |
D. |
a+b>c+d |
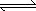 cC(g)+dD(s),ΔH=Q kJ/mol,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示.据图分析,以下说法正确的是
cC(g)+dD(s),ΔH=Q kJ/mol,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示.据图分析,以下说法正确的是