摘要:4.可逆反应mA(s)+nB(g)eC(g)+fD(g).反应过程中.当其他条件不变时.C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列叙述正确的是( ) A.达平衡后.若升温.平衡右移 B.化学方程式中m+n>e+f C.达平衡后.加入催化剂则C%增大 D.达平衡后.增加A的量有利于平衡向右移动 解析:由图象可知.同一温度下随着压强的增大.C的百分含量增大.平衡向右移动.故n>e+f.则m+n>e+f.B正确,同一压强下.温度越低.C的百分含量越大.则升温.平衡左移.A错误,达平衡后.加入催化剂.平衡不移动.则C%不变.C错误,A是固体.增加A的量平衡不移动.D错误. 答案:B
网址:http://m.1010jiajiao.com/timu3_id_84818[举报]
 已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
查看习题详情和答案>>
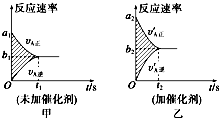 可逆反应mA(g)+nB(g)?pC(g)+qD(g)的v-t图象如图甲,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图乙,以下说法中正确的是( )
可逆反应mA(g)+nB(g)?pC(g)+qD(g)的v-t图象如图甲,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图乙,以下说法中正确的是( )①a1>a2;②a1<a2;③b1>b2;④b1<b2;⑤t1>t2;⑥t1=t2;⑦两图中阴影部分面积相等;⑧图乙中阴影部分面积更大.
查看习题详情和答案>>
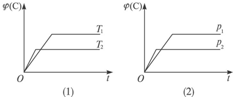 可逆反应mA(s)+nB(g)?eC(g)+fD(g)反应过程中,当其他条件不变时,C的质量分数φ(C)的不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示.则下列叙述正确的是( )
可逆反应mA(s)+nB(g)?eC(g)+fD(g)反应过程中,当其他条件不变时,C的质量分数φ(C)的不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示.则下列叙述正确的是( )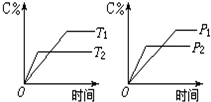 可逆反应mA(s)+nB(g)?pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是( )
可逆反应mA(s)+nB(g)?pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是( )