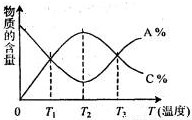
摘要:11.(2010·揭阳市第二次高考模拟)可逆反应aA(g)+bB(s) cC(g)+dD(g).在反应过程中.其他条件不变.C的物质的量分数和T或P关系如图所示.下列叙述中正确的是( ) A.温度降低.化学平衡向逆反应方向移动 B.使用催化剂.C的物质的量分数增加 C.化学方程式系数a<c+d D.无法根据图像确定改变温度后化学平衡移动方向 解析:根据左图所示.T2时达到平衡所需时间短.说明温度T2比T1高.因此降低温度平衡正向移动.加入催化剂.不会移动平衡.根据右图所示.P2时达到平衡所需时间短.说明压强P2比P1大.再分析纵坐标.可以看出压强越大C的物质的量分数越小.即增大压强平衡向n(C) %减小的逆向移动.即a<c+d. 答案:C
网址:http://m.1010jiajiao.com/timu3_id_84727[举报]
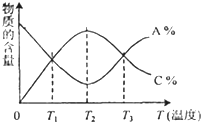 已知可逆反应aA+bB?cC中,物质的含量A%和C%随时间进行、温度的变化曲线如图所示,下列说法正确的是( )
已知可逆反应aA+bB?cC中,物质的含量A%和C%随时间进行、温度的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1温度时已达到过化学平衡 | B、该反应在T3温度时才达到过化学平衡 | C、增大压强平衡一定会向正反应方向移动 | D、该可逆反应的正反应是放热反应 |
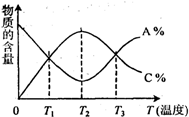 已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )
已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1、T3温度时达到过化学平衡 | B、该反应在T2温度时达到化学平衡 | C、升高温度,平衡会向正反应方向移动 | D、该反应的正反应是放热反应 |
 (2009?肇庆二模)经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( )
(2009?肇庆二模)经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( )