摘要: 在a.b两个烧杯内分别盛有等质量且质量分数相同的稀硫酸.现有两片质量相等的锌片.将其中一片放入a烧杯内.另一片先煅烧成氧化锌后再放入b烧杯内.过一会儿两烧杯内的固体都完全溶解.此时 A. a.b两烧杯中硫酸锌的质量相等 B. a烧杯溶液中硫酸锌的质量分数大 C. b烧杯中硫酸锌的质量大 D. b烧杯溶液中硫酸锌的质量分数大
网址:http://m.1010jiajiao.com/timu3_id_8466[举报]
在a、b两个烧杯内分别盛有等质量且质量分数相同的稀硫酸.现有两片质量相等的锌片,将其中一片放入a烧杯内,另一片先燃烧成氧化锌后再放入b烧杯内.过一会儿两烧杯内的固体都完全溶解,此时
[ ]
A.a、b两烧杯中硫酸锌的质量相等
B.a烧杯溶液与b烧杯溶液中硫酸锌的质量分数相等
C.b烧杯中硫酸锌的质量大
D.b烧杯溶液中硫酸锌的质量分数大
在a、b两个烧杯内分别盛有等质量且质量分数相同的稀硫酸.现有两片质量相等的锌片,将其中一片放入a烧杯内,另一片先煅烧成氧化锌后再放入b烧杯内.过一会儿两烧杯内的固体都完全溶解,此时
A.a、b两烧杯中硫酸锌的质量相等
B.a烧杯溶液中硫酸锌的质量分数大
C.b烧杯中硫酸锌的质量大
D.b烧杯溶液中硫酸锌的质量分数大
托盘天平两盘上,放上A、B两个烧杯,烧杯内均盛有质量不同,但都含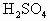 9.8g的稀硫酸,已知A烧杯比B烧杯重.现在A、B两烧杯中分别投入等质量的铁和锌,反应结束后,天平保持平衡.则反应前,A、B两烧杯最大质量差值为________.
9.8g的稀硫酸,已知A烧杯比B烧杯重.现在A、B两烧杯中分别投入等质量的铁和锌,反应结束后,天平保持平衡.则反应前,A、B两烧杯最大质量差值为________.
 (1)高中教材中有这样一个实验:在两支试管中分别加入3mL(足量)稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.(已知:Na2CO3与稀盐酸时先发生:Na2CO3+HCl=NaCl+NaHCO3,然后NaHCO3发生:NaHCO3+HCl=NaCl+H2O+CO2↑)当将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:
(1)高中教材中有这样一个实验:在两支试管中分别加入3mL(足量)稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.(已知:Na2CO3与稀盐酸时先发生:Na2CO3+HCl=NaCl+NaHCO3,然后NaHCO3发生:NaHCO3+HCl=NaCl+H2O+CO2↑)当将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:①试管中(填产生沉淀或气体及反应速率等相关现象)
装有NaHCO3溶液的气球膨胀的较快
装有NaHCO3溶液的气球膨胀的较快
.②盛
NaHCO3溶液
NaHCO3溶液
的试管中气球变得更大,大小气球(包含试管)体积之比约为(填最简整数比)53:42
53:42
;③等质量的两种固体完全反应后生成气体质量不等,但等质量的稀盐酸完全反应后生成气体质量相等,这个结论正确吗?
正确
正确
④综上所述,在泡沫灭火器中常选用
NaHCO3
NaHCO3
来产生CO2(选填NaHCO3或Na2CO3)(2)为研究是吸热还是放热反应,继续进行了下列实验(每个实验各做3次,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| ① | 35mL水 | 2.5gNaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 2.5g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10mL水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 2.5g Na2CO3固体 | 20℃ | 25.1℃ |
①该研究报告的题目是《
NaHCO3、Na2CO3 和盐酸反应过程中热效应的研究
NaHCO3、Na2CO3 和盐酸反应过程中热效应的研究
》②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为
温度计
温度计
和天平
天平
;通过上述实验可得出四条结论:a:NaHCO3 的溶解是
吸热
吸热
(吸热或放热)过程;b:Na2CO3 溶解是
放热
放热
(吸热或放热)过程;c:NaHCO3的饱和溶液和盐酸的反应是
吸热
吸热
(吸热或放热)反应;d:Na2CO3的饱和溶液和盐酸的反应是
放热
放热
(吸热或放热)反应. (1)高中教材中有这样一个实验:在两支试管中分别加入3mL(足量)稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.(已知:Na2CO3与稀盐酸时先发生:Na2CO3+HCl=NaCl+NaHCO3,然后NaHCO3发生:NaHCO3+HCl=NaCl+H2O+CO2↑)当将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:
(1)高中教材中有这样一个实验:在两支试管中分别加入3mL(足量)稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.(已知:Na2CO3与稀盐酸时先发生:Na2CO3+HCl=NaCl+NaHCO3,然后NaHCO3发生:NaHCO3+HCl=NaCl+H2O+CO2↑)当将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:
①试管中(填产生沉淀或气体及反应速率等相关现象)________.
②盛________的试管中气球变得更大,大小气球(包含试管)体积之比约为(填最简整数比)________;
③等质量的两种固体完全反应后生成气体质量不等,但等质量的稀盐酸完全反应后生成气体质量相等,这个结论正确吗?________
④综上所述,在泡沫灭火器中常选用________来产生CO2(选填NaHCO3或Na2CO3)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每个实验各做3次,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| ① | 35mL水 | 2.5gNaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 2.5g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10mL水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 2.5g Na2CO3固体 | 20℃ | 25.1℃ |
①该研究报告的题目是《________》
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为________和________;通过上述实验可得出四条结论:
a:NaHCO3 的溶解是________(吸热或放热)过程;
b:Na2CO3 溶解是________(吸热或放热)过程;
c:NaHCO3的饱和溶液和盐酸的反应是________(吸热或放热)反应;
d:Na2CO3的饱和溶液和盐酸的反应是________(吸热或放热)反应. 查看习题详情和答案>>