网址:http://m.1010jiajiao.com/timu3_id_84497[举报]

(1)图1是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率.电化学合成氨过程的总反应式为:N2+3H2
| ||
| (一定条件) |
阳极反应式为:3H2-6e-=6H+,则阴极反应式为
(3)工业中常用以下反应合成氨:N2+3H2?2NH3△H<0.某实验室在三个不同条件的密闭容器中,分别加入浓度均为c (N2)=0.1mol/L,c (H2)=0.3mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示.
I.该反应实验②平衡时H2的转化率为
II.据图2所示,②、③两装置中各有一个条件与①不同.请指出,并说明判断的理由.③条件:
该反应为放热反应,温度升高,达到平衡的时间缩短,但平衡向逆反应方向移动,③中到达平衡时N2的浓度高于①
该反应为放热反应,温度升高,达到平衡的时间缩短,但平衡向逆反应方向移动,③中到达平衡时N2的浓度高于①
(4)I.NH4Cl溶液呈酸性,这是由于NH4+水解的缘故.则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的离子方程式是
II.常温下,0.1mol?L-1氨水与0.1mol?L-1盐酸溶液等体积混合(忽略混合后溶液体积的变化),则混合溶液中由水电离出的c(H+)


(1)如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递HH+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率.电化学合成氨过程的总反应式为:N2+3H2
| ||
| (一定条件) |
(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)
 2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:(已知K=
2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:(已知K=| C(N2)?[C (H2) ]3 |
| [C (NH3)]2 |
| t/K | 298 | 398 | 498 | … |
| K/(mol?L-1)-2 | 4.1×106 | K1 | K2 | … |
①试确定K1的相对大小,K1
②下列各项能作为判断该反应达到化学平衡状态的依据的是
A.容器内N2、H2、NH3的浓度之比为1:3:2 B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故.则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
D.C(NH4+)>C(Cl-)>C(H+)>C(OH-)
(1)用CH4催化还原NOx可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,则△H2=
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,从而大大提高了氮气和氢气的转化率.电化学合成氨过程的总反应式为:N2+3H2
| ||
| 一定条件 |
(3)在一定条件下,将l mol N2与3mol H2混合于一个10L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,
试回答:①N2的转化率为

②右图中在状态A时,平衡常数 KA
| 0.082 |
| 0.06×0.183 |
| 0.082 |
| 0.06×0.183 |
③在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 时间/min 浓度/mol.L |
c (N2) | c (H2) | c (NH3) |
| 0 | 0.6 | 1.8 | 0 |
| 3 | 0.52 | x | 0.16 |
| 6 | 0.36 | 1.08 | 0.48 |
| 9 | 0.36 | 1.08 | 0.48 |
a.使用催化剂 b.降低温度 c.增加H2的浓度.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为____ _____。

(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递 )实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2
)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2 2NH3,则在电化学合成氨的过程中,阴极反应式为___
______。
2NH3,则在电化学合成氨的过程中,阴极反应式为___
______。
(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
△H<0,其化学平衡常数K与t的关系如下表:
|
t / K |
298 |
398 |
498 |
…… |
|
K / (mol·L-1)-2 |
4.1×106 |
K1 |
K2 |
…… |
请完成下列问题:
①写出Km的表达式 ,判断K1的相对大小,K1_______4.1×106 (填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据是_______(填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B. v(N2)(正) = 3v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
E. 浓度积Q=K时
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故。则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是 。
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为( )
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
D.C(NH4+)>C(Cl-)>C(H+)>C(OH-)
查看习题详情和答案>>
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) = 2 N2(g)+CO2(g) + 2H2O(g) ΔH2
若1 mol CH4 还原NO2 至N2,整个过程中放出的热量为867 kJ,则ΔH2= ;
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:![]() +3
+3![]()
![]() 2
2![]() ,则在电化学合成氨的过程中,阴极反应式为 ;
,则在电化学合成氨的过程中,阴极反应式为 ;
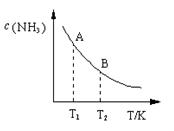
(3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答:
①N2的转化率为 ;
②右图中在状态A时,平衡常数 KA (填写代入数值的表达式,不要求算出具体数值);当温度由T1变化到T2时, KA KB(填“>”、“<”或“=”)。
③在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
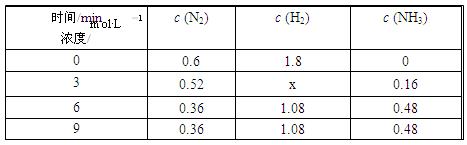
反应从0 min到3 min之间,H2的反应速率为 ;反应在3 min时,条件发生了改变,改变的条件可能是 (填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度
查看习题详情和答案>>