摘要:5.下列化学方程式及其相应的反应类型都正确的是( ) A.乙醇与氧气反应制乙醛 2CH3CH2OH+O2催化剂△2CH3CHO 氧化反应 B.苯与浓硫酸.浓硝酸的混合液共热制硝基苯 取代反应 C.由氯乙烯制取聚氯乙烯树脂 nCH2===CHCl催化剂CH2 加聚反应 D.乙烯使溴的四氯化碳溶液褪色 CH2===CH2+Br2―→CH2BrCH2Br 加成反应 解析:A项中产物漏掉了水.应为:2CH3CH2OH+O2催化剂△2CH3CHO+2H2O,B项中硝基苯的结构错误.应为:HNO3+ 浓硫酸△ +H2O,C项中产物书写错误.应为: nCH2===CHCl催化剂 . 答案:D
网址:http://m.1010jiajiao.com/timu3_id_84368[举报]
下列化学方程式及其相应的反应类型都正确的是
[ ]
A.乙醇与氧气反应制乙醛 2CH3CH2OH+O2 2CH3CHO 氧化反应
2CH3CHO 氧化反应
B.苯与浓硫酸、浓硝酸的混合液共热制硝基苯
 取代反应
取代反应
C.由氯乙烯制取聚氯乙烯树脂 nCH2=CHCl
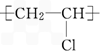 加聚反应
加聚反应
D.乙烯使溴的四氯化碳溶液褪色 CH2=CH2+Br2→CH2BrCH2Br 加成反应
查看习题详情和答案>>
 2CH3CHO 氧化反应
2CH3CHO 氧化反应 B.苯与浓硫酸、浓硝酸的混合液共热制硝基苯
 取代反应
取代反应C.由氯乙烯制取聚氯乙烯树脂 nCH2=CHCl

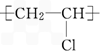 加聚反应
加聚反应 D.乙烯使溴的四氯化碳溶液褪色 CH2=CH2+Br2→CH2BrCH2Br 加成反应
下列化学方程式与相应的离子方程式都正确的是 ( )
A.CuCl2+Fe===FeCl2+Cu Fe+Cu2+===Fe2++Cu
B.2HNO3+CaCO3===Ca(NO3)2+CO2↑+H2O 2H++CO32-===CO2↑+H2O
C.2Fe+6HCl===2FeCl3+3H2↑ 2Fe+6H+===2Fe2++3H2↑
D.Cu(OH)2+2HCl===CuCl2+2 H2O OH-+H+=== H2O
查看习题详情和答案>>(2013?重庆模拟)已知Cl2、Al2(SO4)3、C2H5Br、CH3COOCH3等物质均能与水发生反应,反应时各物质和水均分别离解成两部分,然后再两两重新组合,形成新的物质.下列化学方程式中正确的是( )
①ICl+H2O═HIO+HCl ②CH3COCl+H2O→CH3COOH+HCl
③SiCl4+4H2O═H4SiO4+4HCl ④Mg3N2+6H2O═3Mg(OH)2+2NH3↑
①ICl+H2O═HIO+HCl ②CH3COCl+H2O→CH3COOH+HCl
③SiCl4+4H2O═H4SiO4+4HCl ④Mg3N2+6H2O═3Mg(OH)2+2NH3↑
查看习题详情和答案>>
下列化学方程式书写正确的是( )
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1 | B、氢硫酸在溶液中的电离方程式为H2S???2H++S2- | C、NaHCO3水解的离子方程式为HCO3-+H2O?CO2 3-+H3O+ | D、用双氧水将海带灰处理后的酸性溶液中的I-转变为I2:H2O2+2I-=I2+2OH- |
(2013?辽宁一模)已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,157℃时开始分解.
(1)探究草酸的酸性
25℃H2C2O4 K1=5.4×10-2,K2=5.4×10-5;H2CO3K1=4.5×10-7,K2=4.7×10-11
下列化学方程式可能正确的是
A.H2C2O4+CO32-=HCO3-+HC2O4-B.HC2O4-+CO32-=HCO3-+C2O42-
C.2C2O42-+CO2+H2O=2HC2O4-+CO32-D.H2C2O4+CO32-+=C2O42-+H2O+CO2↑
(2)探究草酸分解产物

①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:
②写出H2C2O4分解的化学方程式:
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mL 0.0lmol/LKMnO4酸性溶液和2mL0.1moL/L H2C2O4溶液,再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀.填写下表:
(4)用酸性KmnO4溶液滴定Na2C2O4,求算Na2C2O4的纯度
实验步骤:准确称取2.0g Na2C2O4固体,配成100mL溶液,取出20.00mL于锥形瓶中.再向瓶中加入足量稀H2SO4,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL.
①高锰酸钾溶液应装在
②滴定至终点时的实验现象是:
③Na2C2O4的纯度是:
查看习题详情和答案>>
(1)探究草酸的酸性
25℃H2C2O4 K1=5.4×10-2,K2=5.4×10-5;H2CO3K1=4.5×10-7,K2=4.7×10-11
下列化学方程式可能正确的是
BD
BD
.A.H2C2O4+CO32-=HCO3-+HC2O4-B.HC2O4-+CO32-=HCO3-+C2O42-
C.2C2O42-+CO2+H2O=2HC2O4-+CO32-D.H2C2O4+CO32-+=C2O42-+H2O+CO2↑
(2)探究草酸分解产物

①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:
吸收CO2气体
吸收CO2气体
,证明有CO气体生成的现象是:F中黑色CuO变成光亮的红色,G中澄清石灰水变浑浊
F中黑色CuO变成光亮的红色,G中澄清石灰水变浑浊
.②写出H2C2O4分解的化学方程式:
H2C2O4
CO2↑+CO↑+H2O↑
| ||
H2C2O4
CO2↑+CO↑+H2O↑
.
| ||
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mL 0.0lmol/LKMnO4酸性溶液和2mL0.1moL/L H2C2O4溶液,再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀.填写下表:
| 反应现象 | 两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快 两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快 |
| 实验结论 | MnSO4(Mn2+)是此反应的催化剂,加入催化剂可以使化学反应速率加快 MnSO4(Mn2+)是此反应的催化剂,加入催化剂可以使化学反应速率加快 |
| 试管中发生反应的离子方程式 | 2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O 2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O |
实验步骤:准确称取2.0g Na2C2O4固体,配成100mL溶液,取出20.00mL于锥形瓶中.再向瓶中加入足量稀H2SO4,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL.
①高锰酸钾溶液应装在
酸式
酸式
滴定管中.(填“酸式”或“碱式”)②滴定至终点时的实验现象是:
滴入最后一滴KMnO4,溶液由无色变为紫色(紫红色)
滴入最后一滴KMnO4,溶液由无色变为紫色(紫红色)
.③Na2C2O4的纯度是:
33.5%
33.5%
.