摘要:12.CO.CH4均为常见的可燃性气体. (1)等体积的CO和CH4在相同条件下分别完全燃烧.转移的电子数之比是 . (2)已知在101 kPa时.CO的燃烧热为283 kJ/mol.相同条件下.若2 mol CH4完全燃烧生成液态水.所放出的热量为1 mol CO完全燃烧放出热量的6.30倍.CH4完全燃烧反应的热化学方程式是 . (3)120℃.101 kPa下.a mL由CO.CH4组成的混合气体在b mL O2中完全燃烧后.恢复到原温度和压强.若混合气体与O2恰好完全反应.产生b mL CO2.则混合气体中CH4的体积分数为 . 解析:(1)CO转化成CO2:化合价从+2→+4,CH4转化成CO2:化合价从-4→+4,所以转移电子数之比为2∶8=1∶4. (3)由方程式:2CO+O2===2CO2, CH4+2O2===CO2+2H2O(g) 当耗O2和生成的CO2相同时.n(CO)∶n(CH4)=2∶1.可知CH4的体积分数是1/3=0.33, 答案:(1)1∶4 (2)CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-891 kJ/mol (3)0.33
网址:http://m.1010jiajiao.com/timu3_id_83905[举报]
CO、CH4均为常见的可燃性气体.
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为
②若燃烧后气体体积缩小了
mL,则a与b关系的数学表达式是
查看习题详情和答案>>
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
1:4
1:4
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是
CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H=-891.45kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H=-891.45kJ/mol
.(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为
0.33
0.33
(保留2位小数).②若燃烧后气体体积缩小了
| a |
| 4 |
b≥
a
| 5 |
| 4 |
b≥
a
.| 5 |
| 4 |
CO、CH4均为常见的可燃性气体.
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是______
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是______.
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为______(保留2位小数).
②若燃烧后气体体积缩小了
mL,则a与b关系的数学表达式是______.
查看习题详情和答案>>
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是______
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是______.
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为______(保留2位小数).
②若燃烧后气体体积缩小了
| a |
| 4 |
CO、CH4均为常见的可燃性气体.
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是________.
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol.相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是__________________________.
(3)120℃、101 kPa下,a mL由CO、CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强.若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为________(保留2位小数).
查看习题详情和答案>>
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是________.
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol.相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是__________________________.
(3)120℃、101 kPa下,a mL由CO、CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强.若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为________(保留2位小数).
CO、CH4均为常见的可燃性气体.
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是 .
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为 (保留2位小数).
②若燃烧后气体体积缩小了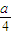 mL,则a与b关系的数学表达式是 .
查看习题详情和答案>>
mL,则a与b关系的数学表达式是 .
查看习题详情和答案>>
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是 .
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为 (保留2位小数).
②若燃烧后气体体积缩小了
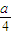 mL,则a与b关系的数学表达式是 .
查看习题详情和答案>>
mL,则a与b关系的数学表达式是 .
查看习题详情和答案>>
CO、CH4均为常见的可燃性气体.
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是________.
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol.相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6
.30倍,CH4完全燃烧反应的热化学方程式是:________.(3)120℃、101 kPa下,a mL由CO、CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强.
①若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为________(保留2位小数).
②若燃烧后气体体积缩小了a/4 mL,则a与b关系的数学表示式是________.