摘要:12.(1)与纯水的电离相似.液氨中也存在着微弱的电离:2NH3NH+NH.据此判断.以下叙述错误的是 ( ) A.液氨中含有NH3.NH.NH等粒子 B.一定温度下液氨中c(NH)·c(NH)是一个常数 C.液氨达到电离平衡时c(NH3)=c(NH)=c(NH) D.只要不加入其他物质.液氨中c(NH)=c(NH) (2)完成下列反应的化学方程式: ①在液氨中投入一小块金属钠.放出气体: . ②NaNH2溶于水的反应: . (3)类似于“H++OH-===H2O 的离子反应: . 解析:(1)据可逆反应的特点知液氨存在NH3.NH与NH三种粒子.A正确,类比水的离子积可知B正确,液氨达到电离平衡时.各粒子的浓度不再改变 .而非相等.C错误,因生成1 mol NH同时生成1 mol NH.故D正确. (2)①类比Na与水的反应.可知Na投入到液氨中反应为2Na+2NH3===2NaNH2+H2↑. ②NaNH2与水发生复分解反应生成NaOH和NH3. (3)完全类比即可写出NH+NH===2NH3. 答案:(1)C (2)①2Na+2NH3===H2↑+2NaNH2 ②NaNH2+H2O===NaOH+NH3↑ (3)NH+NH===2NH3
网址:http://m.1010jiajiao.com/timu3_id_83664[举报]
与纯水的电离相似,液氨中也存在着微弱的电离: 2NH3 ![]() NH4++NH2-,据此判断以下叙述中错误的是:
NH4++NH2-,据此判断以下叙述中错误的是:
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)·C(NH2-)是一个常数
C.液氨的电离到达平衡时C(NH3)=C(NH4+)=C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+)=C(NH2-)
查看习题详情和答案>>与纯水的电离相似,液氨中也存在着微弱的电离: 2NH3 NH4++NH2-,据此判断以下叙述中错误的是:
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)·C(NH2-)是一个常数
C.液氨的电离到达平衡时C(NH3)=C(NH4+)=C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+)=C(NH2-)
查看习题详情和答案>>
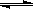 NH4++NH2-,据此判断以下叙述中错误的是:
NH4++NH2-,据此判断以下叙述中错误的是: