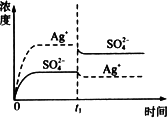
摘要:8.已知Ag2SO4的Ksp为2.0×10-5.将适量Ag2SO4固体溶于100 mL水中至刚好饱和.该过程中Ag+和SO浓度随时间变化关系如右图所示[饱和Ag2SO4溶液中c(Ag+)=0.034 mol/L].若t1时刻在上述体系中加入100 mL 0.020 mol/L Na2SO4溶液.下列示意图中.能正确表示t1时刻后Ag+和SO浓度随时间变化关系的是 ( ) 解析:在饱和Ag2SO4溶液中.c(Ag+)=0.034 mol/L.则c(SO)=0.017 mol/L.加入100 mL 0.020 mol/L Na2SO4溶液后.c(Ag+)=0.017 mol/L, c(SO)==0.0185 mol/L. [c(Ag+)]2·c(SO)=5.3×10-6<2.0×10-5.不会析出Ag2SO4沉淀.则c(Ag+)==0.017 mol/L.B正确. 答案:B
网址:http://m.1010jiajiao.com/timu3_id_83632[举报]
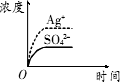
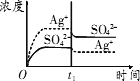
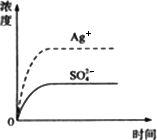
已知Ag2SO4的Ksp为2.0×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO42-浓度随时间变化关系如图所示[饱和Ag2SO4溶液中c(Ag+)=0.034 mol/L].若t1时刻在上述体系中加入100 mL 0.020 mol/L Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是
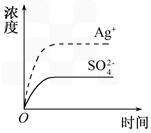
[ ]
A.
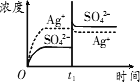
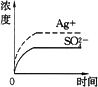
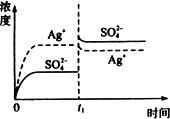
B.
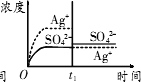
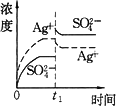
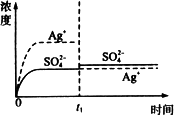
C.
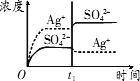
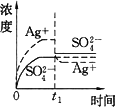
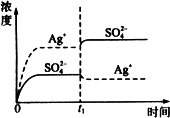
D.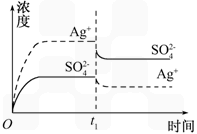
查看习题详情和答案>>

B.

C.

D.

|
已知 Ag2SO4的Ksp为2.0×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO42-浓度随时间变化关系如图[饱和Ag2SO4溶液中c(Ag+)=0.034 mol/L].若t1时刻在上述体系中加入100 mL 0.020 mol/L Na2SO4溶液,下图所示的四个示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是
| |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
已知Ag2SO4的Ksp为2.0×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO42-浓度随时间变化关系如下图(饱和Ag2SO4溶液中c(Ag+)=0.034 mol·L-1).若t1时刻在上述体系中加入100 mL 0.020 mol·L-1 Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是
| |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
已知Ag2SO4的KSP为2.0×10-5,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和
| |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|