网址:http://m.1010jiajiao.com/timu3_id_81942[举报]
2006年5月12日百度网报道,不粘锅的涂层材料聚全氟乙烯可能会导致癌变,建议慎用不粘锅,下列关于聚全氟乙烯的说法正确的是( )
A.聚全氟乙烯是有机物,熔点较低
B.聚全氟乙烯的结构简式可表示为![]()
C.聚全氟乙烯的单体燃烧生成CO2和HF
D.聚全氟乙烯的单体可能使溴水褪色
查看习题详情和答案>>A.聚全氟乙烯是有机物,熔点较低
B.聚全氟乙烯的结构简式可表示为![]()
C.聚全氟乙烯的单体燃烧生成CO2和HF
D.聚全氟乙烯的单体可能使溴水褪色
查看习题详情和答案>>(1)已知在101 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气和H2O,放出热量624 kJ(25 ℃时),N2H4完全燃烧的热化学方程式是______________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式是______________;?
负极的电极反应式是______________。?
(3)下图是一个电解过程示意图。?

①锌片上发生的电极反应式是_____________________。?
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼-空气燃料电池理论上消耗标准状况下的空气_______L(假设空气中氧气体积分数为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式是_____________________。
查看习题详情和答案>>(08安庆模拟)2006年1月12日美国升空的探测器在7月4日与“彗星相撞,产生4.5吨
TNT当量爆炸威力。其火箭推进剂仍然以肼(N2H4)作为主要燃料,NO2为氧化剂,反应生成
N2和水蒸气。已知N2(g)+2O2(g)= 2NO2(g);ΔH= +67.7KJ/mol,
N2H4(g)+O2(g)=N2(g)+2H2O (g);ΔH= ―534KJ/mol。下列关于肼和NO2反映的热化学方程式中,正确的是( )
A. 2 N2H4(g)+2 NO2(g)=3 N2(g)+4H2O (l); ΔH= ―1135.7KJ/mol
B. 2 N2H4(g)+2 NO2(g)=3 N2(g)+4H2O (g); ΔH= ―1000.3KJ/mol
C. N2H4(g)+ NO2(g)=![]() N2(g)+2H2O (l); ΔH= ―1135.7KJ/mol
N2(g)+2H2O (l); ΔH= ―1135.7KJ/mol
D. 2 N2H4(g)+2 NO2(g)=3 N2(g)+4H2O (g); ΔH= ―1135.7KJ/mol
查看习题详情和答案>>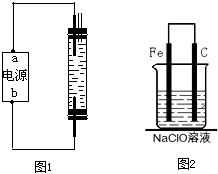 (2010?烟台一模)2008年5月12日我国四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒液,如NaClO溶液.某校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究.
(2010?烟台一模)2008年5月12日我国四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒液,如NaClO溶液.某校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究.甲同学:为制备消毒液,探究并制作了一种家用环保型消毒液(NaClO溶液)发生器,设计了如图1所示的装置,用石墨作电极电解饱和氯化钠溶液.
请完成下列问题:若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a电极名称为
乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用.切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品.本品须密封,置阴凉暗处保存.
请完成以下实验探究过程:
Ⅰ.阅读材料,根据学过的知识判断问题
(1)室温条件下,该消毒液(NaClO)溶液的pH
原因是(用离子方程式表示)
(2)该消毒液还具有的化学性质是
A.强氧化性 B.强还原性 C.不稳定性 D.漂白性 E.弱酸性
Ⅱ.确定要研究的问题
该消毒液对碳钢制品的腐蚀原理.
Ⅲ.设计方案,实施探究
(1)用烧杯取少量样品,将一颗光亮的普通碳钢钉放入烧杯,浸泡一段时间.预期的实验现象是
(2)为了进一步探究碳钢钉在该消毒液(NaClO)中的腐蚀原理,丁同学设计了如图2实验装置,写出碳(C)极上发生的电极反应式