摘要:解决这类题型的方法是:利用原电池两极上的现象.两极上的反应.电子或电流的流向判断出原电池的正负极.再根据负极活动性大于正极的活动性.来比较金属的活动性. 练习1.下图是实验室用氢气还原氧化铜实验的简易装置.其中的铜质燃烧匙可以在试管M中上下移动.实验时,先将细铜丝一端被弯成螺旋状.先在空气中加热变黑后再迅速伸入球型干燥管中. (1)铜质燃烧匙的作用有 . (2)实验过程中.在试管M中可观察到的现象是 . 答案:(1)控制反应的发生和停止,并与锌构成原电池加快反应速率 (2) 铜匙和锌粒表面都由气泡产生, 锌粒逐渐变小或消失. 练习2:燃料电池是目前正在探索的一种新型电池.它可以在燃烧过程中把化学能直接转换为电能.能量的转化率明显高于其它类型的电池.目前已经使用的氢氧燃料电池用多孔铂板做电极.用KOH溶液做电解质溶液.总反应是2H2+O2=2H2O.写出相应的电极反应式 . 答案:正极O2+2H2O+4e-=4OH-, 负极2H2+4OH- -4e- =4H2O.
网址:http://m.1010jiajiao.com/timu3_id_81717[举报]
理查德·赫克、根岸英一和铃木章等三位科学家因在有机合成领域中钯催化交叉偶联反应方面的卓越研究而获得了2010年诺贝尔化学奖。这一成果广泛应用于制药、电子工业和先进材料等领域。碳原子性质不活泼,不会轻易结合,上面三位科学家就是以钯为“媒”撮合碳原子结合在一起。早在一百多年前法国科学家格林尼亚就发明了一种试剂(格氏试剂),利用镁原子强行塞给碳原子两个电子,使碳原子变得活跃。该成果使格林尼亚获得了1912年的诺贝尔化学奖。
已知:
已知:
①格氏试剂的制备: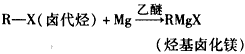
②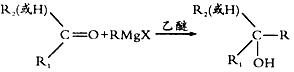
③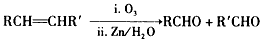
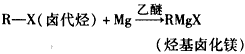
②
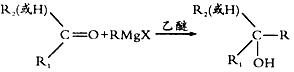
③
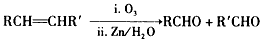
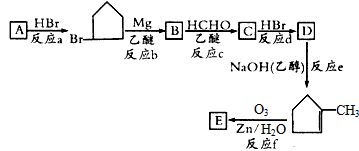
请回答下列问题:
(1)有机化合物A的官能团是________。
(2)B的结构简式是____________。
(3)B生成C的反应中间产物为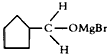 ,该中间产物水解可得C。从有机反应类型看,B生成中间产物
,该中间产物水解可得C。从有机反应类型看,B生成中间产物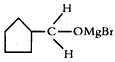 的反应类型属于____________。
的反应类型属于____________。
(4)C生成D的化学方程式为____________________。
(5)该有机合成中从原料物质A到目标产物E碳原子数增加了_____个,增加的碳原子数目决定于____(选择框图中的“反应a”~“反应f”)。
查看习题详情和答案>>
(1)有机化合物A的官能团是________。
(2)B的结构简式是____________。
(3)B生成C的反应中间产物为
 ,该中间产物水解可得C。从有机反应类型看,B生成中间产物
,该中间产物水解可得C。从有机反应类型看,B生成中间产物 的反应类型属于____________。
的反应类型属于____________。(4)C生成D的化学方程式为____________________。
(5)该有机合成中从原料物质A到目标产物E碳原子数增加了_____个,增加的碳原子数目决定于____(选择框图中的“反应a”~“反应f”)。