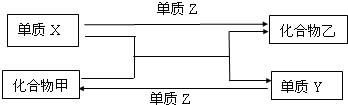
摘要:12.(大庆实验中学高三第四次月考)X.Y.Z是三种短周期元素.甲.乙.丙为化合物.其转化关系如下: 请回答: (1)欲实现右图的转化.在X.Y.Z中最多有 种是金属元素. (2)若甲.乙分子中均含有10个电子.且甲分子中含有3个原子.乙分子中含有4个原子.则乙是 .丙是 . (3)若甲和单质Z均为淡黄色固体.且丙的水溶液显碱性.则甲和水反应的化学方程式为 , X.Y.乙分别是 . . . 已知8 g单质Z完全燃烧放出热量为a kJ.请写出该反应的热化学方程式: . 解析:(1)由转化关系图可知.X.Y.Z三种单质间两两反应.又因为两种金属单质间不发生反应.所以推断X.Y.Z中最多有一中是金属. (2)甲.乙分子中均含有10个电子且分别含有3个原子.4个原子.推测甲为H2O.乙为NH3.那么X.Y.Z分别为O2.H2.N2.则丙为NO. (3)甲为Na2O2.Z为硫.又丙的水溶液显碱性.判断丙是Na2S.X是Na.Y是O2.Z是SO2. 答案:NH3 NO (3)2Na2O2+2H2O===4NaOH+O2↑ Na(钠) O2 SO2+O2(g)===SO2(g),ΔH=-4a kJ/mol.
网址:http://m.1010jiajiao.com/timu3_id_81709[举报]
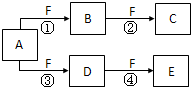 (2011?海淀区二模)X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题:
(2011?海淀区二模)X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示.回答下列问题:(1)Z元素的原子结构示意图为


(2)A的电子式为


HNO3
HNO3
.(3)写出下列反应的化学方程式:①
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
,③
| ||
| △ |
2NH3+3O2
2HNO2+2H2O
| ||
2NH3+3O2
2HNO2+2H2O
.
| ||
(4)A和E反应生成G,Z2Y是一种麻醉剂,由G在210℃分解生成,该分解反应的化学方程式为
NH4NO3
N2O↑+2H2O
| ||
NH4NO3
N2O↑+2H2O
.
| ||
X、Y、Z是三种短周期金属元素,原子序数依次增大,单质的物质的量分别为n(X)、n(Y)、n(Z),它们与足量盐酸反应产生的氢气体积(标准状况下)为V(H2)X、V(H2)Y、V(H2)Z,且n(x)=n(Y)=n(Z),2V(H2)X=V(H2)Y+V(H2)Z.下列说法正确的是( )
查看习题详情和答案>>
 (2012?惠州模拟)X、Y、Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
(2012?惠州模拟)X、Y、Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )