摘要:3.甲酸和乙酸都是弱酸.当它们的浓度均为0.10 mol·L-1时.甲酸中的c(H+)约为乙酸中 c(H+)的3倍.现有两种浓度不等的甲酸溶液 a和b.以及0.10 mol·L-1的乙酸. 经测定它们的pH从大到小依次为a.乙酸.b.由此可知 ( ) A.a的浓度必小于乙酸的浓度 B.a的浓度必大于乙酸的浓度 C.b的浓度必小于乙酸的浓度 D.b的浓度必大于乙酸的浓度 解析:本题主要考查弱电解质的电离平衡知识和酸的相对强弱等问题.由于 c=c(CH3COOH)=0.10 mol·L-1时.甲酸中的c(H+)等于乙酸中c(H+)的3倍.故甲酸的酸性强于乙酸的酸性.又因pH(a)>pH(CH3COOH)>pH(b)即溶液a的c(H+)<0.10 mol·L-1 CH3COOH的c(H+)<溶液b的c(H+).所以a的浓度小于乙酸的浓度.但无法确定乙酸与b的浓度的相对大小(因HCOOH酸性>CH3COOH酸性). 答案:A
网址:http://m.1010jiajiao.com/timu3_id_81685[举报]
甲酸和乙酸都是弱酸,当它们的浓度均为0.10mol/L时,甲酸中的c(H+)约为乙酸中c(H+)的3倍.现有两种浓度不等的甲酸溶液a和b,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为a、乙酸、b.由此可知( )
查看习题详情和答案>>
甲酸和乙酸都是弱酸,当它们的浓度均为0.10 mol·L-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10 mol·L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知
A.a的浓度必小于乙酸的浓度
B.a的浓度必大于乙酸的浓度
C.b的浓度必小于乙酸的浓度
D.b的浓度必大于乙酸的浓度
查看习题详情和答案>>
甲酸和乙酸都是弱酸,当它们的浓度均为0.10 mol·L-1时,甲酸中的[H+]约为乙酸中[H+]的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10 mol·L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知( )
A.a的浓度必小于乙酸的浓度 B.a的浓度必大于乙酸的浓度
C.b的浓度必小于乙酸的浓度 D.b的浓度必大于乙酸的浓度
查看习题详情和答案>>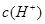 约为乙酸中
约为乙酸中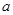 和
和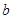 ,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为
,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为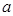 、乙酸、
、乙酸、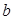 的浓度必小于乙酸的浓度 D、
的浓度必小于乙酸的浓度 D、