摘要:11.如图所示: 淀粉水解可产生某有机化合物A.A在不同的氧化剂作用下.可以生成B(C6H12O7)或C(C6H10O8).B和C都不能发生银镜反应.A.B.C都可以被强还原剂还原成为D(C6H14O6).B脱水可得五元环的酯类化合物E或六元环的酯类化合物F.已知:相关物质被氧化的难易次序是:RCHO最易.R-CH2OH次之. 最难. 请在下列空格中填写A.B.C.D.E.F的结构简式. A ,B ,C ,D ,E ,F . 解析:首先根据A是淀粉的水解产物及A的氧化产物B.C可确定A为葡萄糖.葡萄糖分子结构中有三种结构单元:一个-CHO.一个-CH2OH和四个 .根据题给信息.-CHO最易被氧化.且B的分子组成(C6H12O7)只比CH2OH4CHO多一个O. 所以B是CH2OH4CHO中-CHO被氧化为-COOH的产物. B的结构简式为:CH2OH4COOH.由C的分子组成比葡萄糖多两个O.少两个H可判断除醛基外还有一个醇羟基被氧化.根据题给信息.-CH2OH比 容易被氧化.所以是-CH2OH被氧化为-COOH.C的结构简式为:HOOC4COOH.由D的分子组成可判断.D是CH2OH4CHO中-CHO被还原为-CH2OH的产物.D的结构简式为:CH2OH4CH2OH.B中既有-COOH又有-OH.可以发生分子内酯化反应.生成环状化合物.但-COOH与不同的C上的-OH反应形成的环的大小是不同的.根据E.F是五元环和六元环的酯.可确定E.F分别是-COOH与4.5位C上-OH酯化的产物. 答案:A.CH2OH4CHO B.CH2OH4COOH C.HOOC4COOH D.CH2OH4CH2OH E.CH2OHCHOHHOOHOO F.OHOHOOCH2OHHO
网址:http://m.1010jiajiao.com/timu3_id_81641[举报]
 化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示( )
化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示( )| A、每生成2mol AB(g)吸收b kJ热量 | B、反应热△H=+(a-b)kJ/mol | C、该反应中反应物的总能量小于生成物的总能量 | D、断裂1molA-A键和1molB-B键,放出a kJ能量 |
 某无色格液中只含有NH4+、K+ Al3+ Cu2+、Mg2+、CO32-、SO42-等离子中的几种,(1)取100mL该溶液,滴加足量稀硝酸酸化的Ba(NO3)2溶液,过滤得到0.03mol白色沉淀
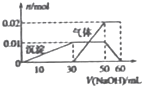
某无色格液中只含有NH4+、K+ Al3+ Cu2+、Mg2+、CO32-、SO42-等离子中的几种,(1)取100mL该溶液,滴加足量稀硝酸酸化的Ba(NO3)2溶液,过滤得到0.03mol白色沉淀(2)另取10mL该洛液于试管中,逐滴加人NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热).最后沉淀完全溶解.沉淀和气体的物质的量与所加NaOH溶液体积的变化关系如图所示( )
| A、溶液中一定不含有Cu2+、Mg2+、CO32-可能含有K+ | B、NH4+、Al3+、SO42-三种离子的物质的量之比为2:1:3 | C、实验中所用的NaOH溶液的物质的量浓度为0.1mol/L | D、只能通过焰色反应实验来确认该溶液中是否存在K+ |
一带有活塞的密封容器中盛有A、B组成的混合气体,在通常条件下,从状态I反应到状态II时,气体体积(V)与气体压强(P)的变化曲线如图所示。

则反应:A(g)+B(g)=2C(g)
A.是放热反应 B.反应后气体总分子数增多
C.是吸热反应 D.反应物具有的总能量等于生成物具有的总能量
查看习题详情和答案>>已知甲和乙在溶液中的转化关系如图所示:
请回答下列问题:
(1)若甲是10电子的单核微粒,乙是两性氢氧化物,则微粒甲的结构示意图为 。
(2)若甲是10电子的阳离子,乙是碱性气体。1mol乙通入足量强酸溶液中与H+反应,反应过程中能量变化如下图:
写出乙的一种用途: ;
该反应的热化学方程式是___________________________。
(3)若甲是CrO42-(黄色)和Cr2O72-(橙色)的混合溶液,在该溶液中存在如下平衡:
CrO42-(黄色) + 2H+ Cr2O72-(橙色) + H2O
Cr2O72-(橙色) + H2O
若测得甲溶液的pH=1,该溶液显 色。
(4)若甲仅含有NO3-、SO42-和X三种离子,则X离子可能是 (填序号) 。
| A.Fe2+ | B.HCO3- | C.Ba2+ | D.Fe3+ |
则HCO3-的电离平衡常数Ka= 。 查看习题详情和答案>>
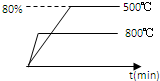 一定条件下,在1L恒容容器中充入2mol A、1mol B,发生反应:
一定条件下,在1L恒容容器中充入2mol A、1mol B,发生反应: