网址:http://m.1010jiajiao.com/timu3_id_81406[举报]
(12分)某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定:①用 式滴定管盛装ca mol/L盐酸标准液。右图
表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的
标准盐酸的体积填入③表空格中。滴定管中剩余液体的体积
25.10mL(填大于、小于或者等于)。
②下表是3种常见指示剂的变色范围:
| 指示剂 | 石蕊 | 甲基橙 | 酚酞 |
| 变色范围(pH) | 5.0—8.0 | 3.1—4.4 | 8.2—10.0 |
该实验可选用 作指示剂;
③有关数据记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.12 | 24.62 |
| 2 |
|
|
|
|
| 3 | V | 6.00 | 30.58 | 24.58 |
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)
cb= 。
(3)下列几种情况会使测定结果偏高的是
a.若滴定前用蒸馏水冲洗锥形瓶;
b.读数时,若滴定前仰视,滴定后俯视;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外;
d.若未充分振荡,刚看到溶液变色,立刻停止滴定。
查看习题详情和答案>>
(12分)某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。

(1)滴定:①用 式滴定管盛装ca mol/L盐酸标准液。右图
表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的
标准盐酸的体积填入③表空格中。滴定管中剩余液体的体积
25.10mL(填大于、小于或者等于)。
②下表是3种常见指示剂的变色范围:
|
指示剂 |
石蕊 |
甲基橙 |
酚酞 |
|
变色范围(pH) |
5.0—8.0 |
3.1—4.4 |
8.2—10.0 |
该实验可选用 作指示剂;
③有关数据记录如下:
|
滴定序号 |
待测液体积(mL) |
所消耗盐酸标准液的体积(mL) |
||
|
滴定前 |
滴定后 |
消耗的体积 |
||
|
1 |
V |
0.50 |
25.12 |
24.62 |
|
2 |
|
|
|
|
|
3 |
V |
6.00 |
30.58 |
24.58 |
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)
cb= 。
(3)下列几种情况会使测定结果偏高的是
a.若滴定前用蒸馏水冲洗锥形瓶;
b.读数时,若滴定前仰视,滴定后俯视;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外;
d.若未充分振荡,刚看到溶液变色,立刻停止滴定。
查看习题详情和答案>>
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定:①用 式滴定管盛装c mol/L盐酸标准液。如图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入③表空格中,此时滴定管中液体的体积 mL。
②下表是4种常见指示剂的变色范围: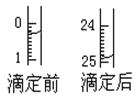
| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0—8.0 | 3.1—4.4 | 4.4—6.2 | 8.2—10.0 |
该实验应选用 作指示剂;
③有关数据记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | | | |
| 3 | V | 6.00 | 31.35 | 25.35 |
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)c = 。
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
A.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果 ;
B.读数时,若滴定前仰视,滴定后俯视,则会使测定结果 ;
C.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果 ;
D.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果 。 查看习题详情和答案>>
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定:①用_______式滴定管盛装c mol/L盐酸标准液。右图表示某 次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入③表空格中,此时滴定管中液体的体积__________mL。
次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入③表空格中,此时滴定管中液体的体积__________mL。
②下表是4种常见指示剂的变色范围:
指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
变色范围(pH) | 5.0―8.0 | 3.1―4.4 | 4.4―6.2 | 8.2―10.0 |
该实验应选用________作指示剂;
③有关数据记录如下:
滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
滴定前 | 滴定后 | 消耗的体积 | ||
1 | V | 0.50 | 25.80 | 25.30 |
2 | V |
|
|
|
3 | V | 6.00 | 31.35 | 25.35 |
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)
c = ______________________________。
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果__________;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果__________;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果__________;
d.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果__________。
查看习题详情和答案>> 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定:①用 式滴定管盛装ca mol/L盐酸标准液。右图
表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的
标准盐酸的体积填入③表空格中。滴定管中剩余液体的体积
25.10mL(填大于、小于或者等于)。
②下表是3种常见指示剂的变色范围:
| 指示剂 | 石蕊 | 甲基橙 | 酚酞 |
| 变色范围(pH) | 5.0—8.0 | 3.1—4.4 | 8.2—10.0 |
该实验可选用 作指示剂;
③有关数据记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.12 | 24.62 |
| 2 |
| |||
| 3 | V | 6.00 | 30.58 | 24.58 |
(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)
cb= 。
(3)下列几种情况会使测定结果偏高的是
a.若滴定前用蒸馏水冲洗锥形瓶;
b.读数时,若滴定前仰视,滴定后俯视;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外;
d.若未充分振荡,刚看到溶液变色,立刻停止滴定。
查看习题详情和答案>> V
V