网址:http://m.1010jiajiao.com/timu3_id_81350[举报]
(15分)已知X是中学化学中常见的盐,其溶液呈蓝色。构成化合物F的两种元素的原子均可形成与氖原子相同电子层结构的离子,化合物F具有强氧化性。M是常见的金属单质,固体E为红棕色,是常用的颜料。N的氧化物可作为耐火材料。D与H都为气体,且两者相遇会出现红棕色。各物质的转化关系如图所示(部分反应产物已略去)。

(1)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是____________________。
(2)写出反应②的离子反应方程式:_________________________________________。
(3)D的化学式为________;X的化学式为______ __;F的电子式为___ __。
(4)用石墨作电极电解1 L X溶液,电解一段时间后,将阴极取出,洗涤、干燥、称量,电极增重3.2 g。则阳极的电极反应式为____________________________________,
 电解后溶液的pH为________(假设电解前后溶液体积不变)。
电解后溶液的pH为________(假设电解前后溶液体积不变)。
(5)反应④的离子方程式为_____________________________________________。
(6)配制A溶液时,需要加入少量的________,其目的是________________________。
查看习题详情和答案>>
已知X是中学化学中常见的盐,其溶液呈蓝色。构成化合物F的两种元素的原子均可形成与氖原子相同电子层结构的离子,化合物F具有强氧化性。M是常见的金属单质,固体E为红棕色,是常用的颜料。N的氧化物可作为耐火材料。D与H都为气体,且两者相遇会出现红棕色。各物质的转化关系如图所示(部分 反应产物已略去)。
反应产物已略去)。
(1)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是____________________。
(2)写出反应②的离子反应方程式:_________________________________________。
(3)D的化学式为________;X的化学式为______ __;F的电子式为___ __。
(4)用石墨作电极电解1 L X溶液,电解一段时间后,将阴极取出,洗涤、干燥、称量,电极增重3.2 g。则阳极的电极反应式为____________________________________,
电解后溶液的pH为________(假设电解前后溶液体积不变)。
( 5)反应④的离子方程式为__________________________________________
5)反应④的离子方程式为__________________________________________ ___。
___。
(6)配制A溶液时,需要加入少量的________,其目的是________________________。
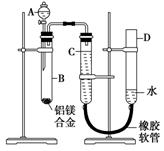
(15分)已知X是中学化学中常见的盐,其溶液呈蓝色。构成化合物F的两种元素的原子均可形成与氖原子相同电子层结构的离子,化合物F具有强氧化性。M是常见的金属单质,固体E为红棕色,是常用的颜料。N的氧化物可作为耐火材料。D与H都为气体,且两者相遇会出现红棕色。各物质的转化关系如图所示(部分反应产物已略去)。
(1)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是____________________。
(2)写出反应②的离子反应方程式:_________________________________________。
(3)D的化学式为________;X的化学式为______ __;F的电子式为___ __。
(4)用石墨作电极电解1 L X溶液,电解一段时间后,将阴极取出,洗涤、干燥、称量,电极增重3.2 g。则阳极的电极反应式为____________________________________,
 电解后溶液的pH为________(假设电解前后溶液体积不变)。
电解后溶液的pH为________(假设电解前后溶液体积不变)。
(5)反应④的离子方程式为_____________________________________________。
(6)配制A溶液时,需要加入少量的________,其目的是________________________。
查看习题详情和答案>>
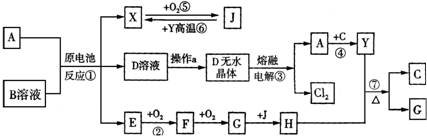
上图中H的浓溶液与炽热的Y单质发生反应⑦,生成C、G的同时也生成了J.请根据图示回答下列问题:
(1)金属A为
(2)写出E的电子式
(3)写出反应⑦的化学方程式
(4)原电池①的总反应为
(5)写出反应②的化学方程式
 A、B、C、X是中学化学中常见的物质,它们之间的转化关系如下图所示(部分产物已略去).请回答下列问题:
A、B、C、X是中学化学中常见的物质,它们之间的转化关系如下图所示(部分产物已略去).请回答下列问题:(1)若X是强氧化性单质,则A不可能是
a.C b.N2 c.S d.Mg e.Al
(2)若A能使湿润的红色石蕊试纸变蓝,C为红棕色的气体.A转化为B的化学方程式为
(3)若X是金属单质,向B、C溶液中分别滴加AgNO3溶液,均产生不溶于稀硝酸的白色沉淀,则B的化学式为
(4)若A、B、C均为含有铝元素的化合物,若X为NaOH溶液,则A与X生成B的离子方程式