网址:http://m.1010jiajiao.com/timu3_id_80943[举报]
下列说法正确的是
A.二氧化锰具有强氧化性,可用作H2O2分解的氧化剂
B.二氧化硫和氯水均具有漂白性,两者混合使用将增强漂白效果
C.在盛放食品的包装袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质
D.锌与稀硫酸反应时加入几滴硫酸铜溶液可加快反应速率,原因是硫酸铜作催化剂
查看习题详情和答案>>
A.戊二醛分子式为C5H8O2,符合此分子式的二元醛有5种
B.1 mol戊二醛与足量的银氨溶液反应,最多可得2 mol单质银
C.戊二醛不能使酸性高锰酸钾溶液褪色
D.戊二醛经催化氧化可以得到的戊二酸有4种同分异构体
查看习题详情和答案>>下列说法正确的是
A.二氧化锰具有强氧化性,可用作H2O2分解的氧化剂
B.二氧化硫和氯水均具有漂白性,两者混合使用将增强漂白效果
C.在盛放食品的包装袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质
D.锌与稀硫酸反应时加入几滴硫酸铜溶液可加快反应速率,原因是硫酸铜作催化剂
查看习题详情和答案>>
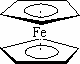
二茂铁[(C5H5)2Fe] 分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法正确的是

A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
B.1mol环戊二烯( )中含有σ键的数目为5NA
)中含有σ键的数目为5NA
C.分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d44s2
查看习题详情和答案>>
|
二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如下图所示,下列说法正确的是
| |
A. |
二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 |
B. |
1 mol环戊二烯( |
C. |
Fe2+的价电子排布式为1s22s22p63s23p63d44s2 |
D. |
分子中存在π键 |