网址:http://m.1010jiajiao.com/timu3_id_80779[举报]
14.依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。
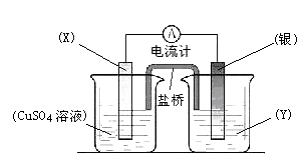
请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;
X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
查看习题详情和答案>>
依据氧![]() 化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池
化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池
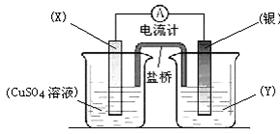
如图所示。请回答![]() 下列问题:
下列问题:
![]() (1)电极X的材料是________;电解质溶液Y[来源:学#科#网]
(1)电极X的材料是________;电解质溶液Y[来源:学#科#网]
是_________;
(2)银电极为电池的___________极,发生的
电极反应为______________;X电极上发
生的电极反应_____________________;
(3)外电路中的电子是从__________电极流向
_____________电极。
查看习题详情和答案>>(9分)依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq)+ 2Ag(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是_________;电解质溶液Y是_________;
(2)银电极为电池的_________极,发生的电极反应为________________________;X电极上发生的电极反应为___________________________;
(3)外电路中的电子是从_________电极流向_________电极。
查看习题详情和答案>>
依据氧化还原反应:2Ag+(aq) + Cu(s) ="=" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。下列说法不正确的是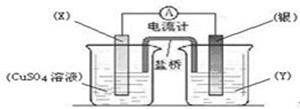
| A.电极X的材料是铜 |
| B.电解质溶液Y是硝酸银溶液; |
| C.银电极为电池的正极,发生的电极反应为:Ag+ + e- ="=" Ag |
| D.盐桥中的阳离子向硫酸铜溶液中运动 |
