摘要:19.先化简.再求值: . 其中 .
网址:http://m.1010jiajiao.com/timu3_id_8036[举报]
老师为同学们提供了如下实验装置:

(1)写出带有标号的仪器名称:a______.
(2)实验室用高锰酸钾制取氧气的发生装置是______(填字母).用排水集气法收集氧气完毕后,正确的操作顺序是______(填字母)
A.先停止加热,再把导管提离水面 B.先把导管提离水面,再停止加热.
(3)都可用于收集CO2和O2的装置是______.
(4)某气体能用BD装置制取,写出制取该气体的化学方程式______.
(5)小伟设计了如图所示的装置对二氧化碳的性质进行探究(固定装置已略去,且石灰石中杂质不反应).
①图缺少了橡皮塞和导管的一部分,请补充完整.
②写出乙试管中发生反应的化学方程式:______.
③小伟观察到乙试管中紫色石蕊溶液变红,使其变红的原因可能是二氧化碳与水反应生成了碳酸,此外还有可能的原因是______.
查看习题详情和答案>>
已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式
(1)先写元素符号(正前负后)
(2)标出各元素的化合价(正上方)
(3)把化合价数值化为最简
(4)把化简后的数字交叉写出(求最小公倍数)
查看习题详情和答案>>
(1)先写元素符号(正前负后)
(2)标出各元素的化合价(正上方)
(3)把化合价数值化为最简
(4)把化简后的数字交叉写出(求最小公倍数)
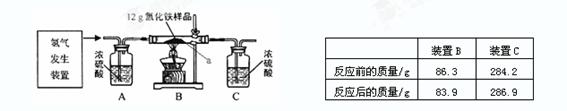
 某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:氢气和氧化铁在高温条件下发生置换反应,杂质不参加反应,浓硫酸具有吸水性,假定每步均完全反应或吸收).
某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:氢气和氧化铁在高温条件下发生置换反应,杂质不参加反应,浓硫酸具有吸水性,假定每步均完全反应或吸收).主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入干燥的氢气; ③点燃B处酒精灯; ④反应结束熄灭B处酒精灯;
⑤待装置B冷却至室温再停止通氢气; ⑥再次称量必要装置的质量.
| 装置B | 装置C | |
| 反应前的质量/g | 86.3 | 286.9 |
| 反应后的质量/g | 83.9 | 284.2 |
玻璃管
玻璃管
.(2)实验时先通氢气后加热的目的是
除去装置内的氧气,防止发生爆炸
除去装置内的氧气,防止发生爆炸
,验证该步骤目的达到的实验方法是收集尾气靠近燃着的酒精灯,听声音
收集尾气靠近燃着的酒精灯,听声音
.(3)装置B处的现象
红色粉末变为黑色
红色粉末变为黑色
.(4)实验结束为什么先停止加热,待装置B冷却至室温再停止通氢气
防止温度降低,C中液体被倒吸入B中
防止温度降低,C中液体被倒吸入B中
.(5)请计算样品中氧化铁的质量分数.(写出计算步骤,计算结果精确到0.l%)
(6)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为
【(286.9g-284.2g)-(86.3g-83.9g)】:(86.3g-83.9g)
【(286.9g-284.2g)-(86.3g-83.9g)】:(86.3g-83.9g)
(不用化简);若氧化铁没有完全反应,则求得水中氢、氧元素的质量比会不变
不变
(“偏大”、“偏小”或“不变”),若缺少装置A,则偏大
偏大
.某同学为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:氢气和氧化铁在高温条件下发生置换反应,杂质不参加反应,浓硫酸具有吸水性,假定每步均完全反应或吸收)。
主要实验步骤如 下:
下:
①按顺序组装仪器,检查装置的气密性,称量样品和必 要装置的质量;②缓缓通入干燥的氢气;③点燃B处酒精灯;④反应结束熄灭B处酒精灯;⑤待装置B冷却至室温再停止通氢气;⑥再次称量必要装置的质量。
要装置的质量;②缓缓通入干燥的氢气;③点燃B处酒精灯;④反应结束熄灭B处酒精灯;⑤待装置B冷却至室温再停止通氢气;⑥再次称量必要装置的质量。
(1)实验时先通氢气后加热的目的是 。验证该步骤目的达到的实验方法是 。
(2)装置B处的现象 发生反应的化学方程式
(3)请计算样品中氧化铁的质量分数
(4)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为 (不用化简);若氧化铁没有完全反应,则求得水中氢、氧元素的质量比会 (“偏大” 、“偏小”或“不变”);若缺少装置A,则求得水中氢、氧元素的质量比会 (“偏大”、“偏小”或“不变”)
、“偏小”或“不变”);若缺少装置A,则求得水中氢、氧元素的质量比会 (“偏大”、“偏小”或“不变”)