摘要:18.计算: |-2| + ÷ .
网址:http://m.1010jiajiao.com/timu3_id_8035[举报]
过碳酸钠广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习:
[资料卡片]:
Ⅰ、制备研究:如图1是制备过碳酸钠的工艺流程.

请回答问题:
(1)反应器中发生反应的化学方程式为______;
(2)生产中,反应及干燥均需在较低温度下进行,原因是______;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为______.
(4)操作A的名称是______,若在实验室完成此操作,需要的玻璃仪器是烧杯、______和______;
(5)洗涤过碳酸钠晶体最好选用______.
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是______和______;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.
小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
[实验步骤]:①______;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中______时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.
[实验分析及数据处理]:
(7)完善实验步骤的相关内容:①______、④______;
(8)实验中,水的作用是______;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是______(填化学式);
(9)实验中,______,则开始收集气体;
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL,计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr=314、Mr(O2)=32]______;
[实验反思]:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是______;
(12)量筒中长导管的作用是______;
(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由.______;
(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为______.
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数?______.(只需给出简要的方案)
查看习题详情和答案>>
[资料卡片]:
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解; |

请回答问题:
(1)反应器中发生反应的化学方程式为______;
(2)生产中,反应及干燥均需在较低温度下进行,原因是______;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为______.
(4)操作A的名称是______,若在实验室完成此操作,需要的玻璃仪器是烧杯、______和______;
(5)洗涤过碳酸钠晶体最好选用______.
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是______和______;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.
小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
[实验步骤]:①______;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中______时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.
[实验分析及数据处理]:
(7)完善实验步骤的相关内容:①______、④______;
(8)实验中,水的作用是______;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是______(填化学式);
(9)实验中,______,则开始收集气体;
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL,计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr=314、Mr(O2)=32]______;
[实验反思]:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是______;
(12)量筒中长导管的作用是______;
(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由.______;
(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为______.
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数?______.(只需给出简要的方案)
查看习题详情和答案>>
过碳酸钠广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习:
[资料卡片]:
Ⅰ、制备研究:如图1是制备过碳酸钠的工艺流程.

请回答问题:
(1)反应器中发生反应的化学方程式为______;
(2)生产中,反应及干燥均需在较低温度下进行,原因是______;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为______.
(4)操作A的名称是______,若在实验室完成此操作,需要的玻璃仪器是烧杯、______和______;
(5)洗涤过碳酸钠晶体最好选用______.
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是______和______;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.
小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
[实验步骤]:①______;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中______时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.
[实验分析及数据处理]:
(7)完善实验步骤的相关内容:①______、④______;
(8)实验中,水的作用是______;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是______(填化学式);
(9)实验中,______,则开始收集气体;
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL,计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr=314、Mr(O2)=32]______;
[实验反思]:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是______;
(12)量筒中长导管的作用是______;
(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由.______;
(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为______.
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数?______.(只需给出简要的方案)
查看习题详情和答案>>
[资料卡片]:
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解; |

请回答问题:
(1)反应器中发生反应的化学方程式为______;
(2)生产中,反应及干燥均需在较低温度下进行,原因是______;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为______.
(4)操作A的名称是______,若在实验室完成此操作,需要的玻璃仪器是烧杯、______和______;
(5)洗涤过碳酸钠晶体最好选用______.
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是______和______;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.
小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
[实验步骤]:①______;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中______时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.
[实验分析及数据处理]:
(7)完善实验步骤的相关内容:①______、④______;
(8)实验中,水的作用是______;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是______(填化学式);
(9)实验中,______,则开始收集气体;
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL,计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr=314、Mr(O2)=32]______;
[实验反思]:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是______;
(12)量筒中长导管的作用是______;
(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由.______;
(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为______.
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数?______.(只需给出简要的方案)
查看习题详情和答案>>
过碳酸钠广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习:
[资料卡片]:
Ⅰ、制备研究:如图1是制备过碳酸钠的工艺流程.

请回答问题:
(1)反应器中发生反应的化学方程式为______;
(2)生产中,反应及干燥均需在较低温度下进行,原因是______;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为______.
(4)操作A的名称是______,若在实验室完成此操作,需要的玻璃仪器是烧杯、______和______;
(5)洗涤过碳酸钠晶体最好选用______.
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是______和______;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.
小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
[实验步骤]:①______;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中______时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.
[实验分析及数据处理]:
(7)完善实验步骤的相关内容:①______、④______;
(8)实验中,水的作用是______;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是______(填化学式);
(9)实验中,______,则开始收集气体;
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL,计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr=314、Mr(O2)=32]______;
[实验反思]:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是______;
(12)量筒中长导管的作用是______;
(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由.______;
(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为______.
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数?______.(只需给出简要的方案)
查看习题详情和答案>>
[资料卡片]:
| 1、过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热、遇水易分解; 2、过碳酸钠分解的化学方程式为2=4 Na2CO3+6 H2O+3O2↑ 3、H2O2分解放出热量,Na2CO3受热不分解; |

请回答问题:
(1)反应器中发生反应的化学方程式为______;
(2)生产中,反应及干燥均需在较低温度下进行,原因是______;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为______.
(4)操作A的名称是______,若在实验室完成此操作,需要的玻璃仪器是烧杯、______和______;
(5)洗涤过碳酸钠晶体最好选用______.
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是______和______;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.
小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
[实验步骤]:①______;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中______时,停止滴加水,并关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算.
[实验分析及数据处理]:
(7)完善实验步骤的相关内容:①______、④______;
(8)实验中,水的作用是______;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是______(填化学式);
(9)实验中,______,则开始收集气体;
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL,计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数[Mr=314、Mr(O2)=32]______;
[实验反思]:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是______;
(12)量筒中长导管的作用是______;
(13)有同学提出,装置中原有空气会使测定结果偏大.这种说法是否正确,如不正确,请说明理由.______;
(14)经过讨论,小组同学一致认为可用下述方案进行测定.方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g.则样品中2Na2CO3?3H2O2的质量分数为______.
(15)根据资料卡片,你还能设计出什么方案测定样品中2Na2CO3?3H2O2的质量分数?______.(只需给出简要的方案)
查看习题详情和答案>>
如图是实验室制取气体的一些装置,据图回答有关问题.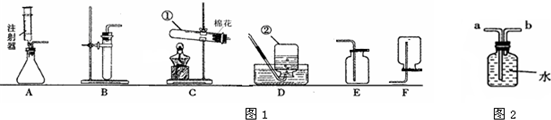
(1)写出序号为①②的仪器名称:①______;②______.
(2)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5;
②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;
③将带火星的木条依次插入1~5号瓶中,把观察到现象和计算数据,填入下表.
| 集气瓶标号 | 1 | 2 | 3 | 4 | 5 |
| 集气瓶中氧气的体积分数 | 28.9% | 36.8% | 44.7% | 52.6% | 60.5% |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,发生装置选用______,其收集装置选用______反应的文字表达式是______,该反应所属的基本反应类型是______.
②根据以上实验,下列说法中正确的是______(填写相应的标号).
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条才能复燃
C.只要有氧气存在就可使带火星的木条复燃
D.集气瓶中氧气的浓度越大,带火星的木条就越容易复燃
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是______;如果用如图所示装置收集乙炔,气体应从______(填“a”或“b”)端管口通入. 查看习题详情和答案>>
如图是实验室制取气体的一些装置,据图回答有关问题.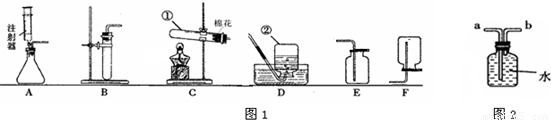
(1)写出序号为①②的仪器名称:① ;② .
(2)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5;
②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;
③将带火星的木条依次插入1~5号瓶中,把观察到现象和计算数据,填入下表.
试回答下列问题:
①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,发生装置选用 ,其收集装置选用 反应的文字表达式是 ,该反应所属的基本反应类型是 .
②根据以上实验,下列说法中正确的是 (填写相应的标号).
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条才能复燃
C.只要有氧气存在就可使带火星的木条复燃
D.集气瓶中氧气的浓度越大,带火星的木条就越容易复燃
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是 ;如果用如图所示装置收集乙炔,气体应从 (填“a”或“b”)端管口通入. 查看习题详情和答案>>

(1)写出序号为①②的仪器名称:① ;② .
(2)某学校化学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取5只250mL集气瓶,分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5;
②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1~5号瓶中的水排去;
③将带火星的木条依次插入1~5号瓶中,把观察到现象和计算数据,填入下表.
| 集气瓶标号 | 1 | 2 | 3 | 4 | 5 |
| 集气瓶中氧气的体积分数 | 28.9% | 36.8% | 44.7% | 52.6% | 60.5% |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
①实验室中采用分解过氧化氢(H2O2)的方法制取氧气,发生装置选用 ,其收集装置选用 反应的文字表达式是 ,该反应所属的基本反应类型是 .
②根据以上实验,下列说法中正确的是 (填写相应的标号).
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条才能复燃
C.只要有氧气存在就可使带火星的木条复燃
D.集气瓶中氧气的浓度越大,带火星的木条就越容易复燃
(3)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是 ;如果用如图所示装置收集乙炔,气体应从 (填“a”或“b”)端管口通入. 查看习题详情和答案>>