网址:http://m.1010jiajiao.com/timu3_id_80008[举报]
拟用如图所示装置制取如下表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去,必要时可以加热,a、b、c、d表示相应仪器中加入的试剂).

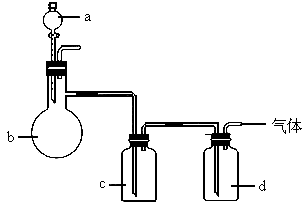
(1)上述方法中可以得到干燥、纯净的________________________气体.
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满).
①气体_____________________________________________________,
理由:_____________________________________________________.
②气体_____________________________________________________,
理由:_____________________________________________________.
③气体_____________________________________________________,
理由:_____________________________________________________.
④气体_____________________________________________________,
理由:_____________________________________________________.
查看习题详情和答案>>拟用如图所示装置制取如下表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去,必要时可以加热,a、b、c、d表示相应仪器中加入的试剂).

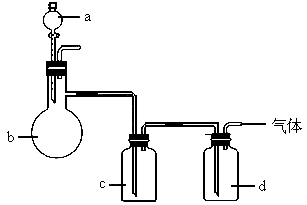
(1)上述方法中可以得到干燥、纯净的________________________气体.
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满).
①气体_____________________________________________________,
理由:_____________________________________________________.
②气体_____________________________________________________,
理由:_____________________________________________________.
③气体_____________________________________________________,
理由:_____________________________________________________.
④气体_____________________________________________________,
理由:_____________________________________________________.
查看习题详情和答案>>
(1)实验室制取氨气的化学方程式为 ,工业上合成氨采取的下列措施中可用勒夏特列原理解释的是? ?(填字母)?
A.采用较高压强(20 Mpa~50 Mpa)?
B.采用500 ℃的高温?
C.用铁触媒作催化剂?
D.将生成的氨液化并及时从体系中分离出来,N2和H2循环到合成塔中并补充N2和H2?
(2)适当改变如图所示的装置后,也可用来制取和收集氧气。改变的方法是: 。?
(3)实验室用浓硫酸和铜制取并收集少量的SO2气体,能否采用该装置 ? ?(填“能”或“不能”),若选填“能”,请说明理由;若选填“不能”,则怎样改变该装置后就能达到实验目的?请用文字说明 ;?
(4)取6.4 g铜片和12 mL 18.4 mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,某同学根据所学的化学知识认为还有一定量的硫酸剩余。下列药品能够用来证明反应结束后烧瓶中确实有余酸的是?? ??(填字母)。?
A.铁粉 B.氯化钡溶液? C.银粉 D.碳酸氢钠溶液?
(5)为定量测定余酸物质的量浓度,某同学进行了如下设计:先测定铜片与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度。测定SO2的量的方案很多,下列方案可行的
是 (填字母)?
A.将装置中产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量?
B.将装置中产生的气体缓缓通入足量氢氧化钡溶液,反应完全后过滤、洗涤、干操、称量沉淀?
C.将装置中产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后过滤、洗涤、干燥、称量沉淀?
请对不可行的方案进行分析(可以不填满)
方案序号 | 分析 | 误差(偏高或偏低) |
|
|
|
|
|
|
|
|
|
(6)请再设计其他可行的实验方案来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)。??
查看习题详情和答案>> 某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.
某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.(1)利用Ⅰ、Ⅱ装置可制取收集气体(K2关闭,K1打开)
①下列各组物质中能直接利用这套装置进行实验的是
A.锌和稀硫酸B.双氧水和二氧化锰C.浓氨水和氧化钙D.浓盐酸和二氧化锰
②在不改变Ⅰ、Ⅱ装置及位置的前提下,若要制取收集NO气体,可采取的改进方法是装置Ⅱ内充满水;若要制取收集NO2气体,可采取的改进方法是:
(2)利用Ⅰ、Ⅲ装置可验证物质的性质(K2打开,K1关闭)
①若要证明氧化性:KMnO4>Cl2>Br2,则A中加浓盐酸,B中加KMnO4,C中发生的离子反应方程式
②若要证明乙炔为不饱和烃,则I中发生的化学反应方程式为:
C中的现象为
(3)装置Ⅲ中使用球形干燥管D可防止液体倒吸,其原因是
