摘要:10.对于平衡体系:mA(g)+nB(g) pC(g)+qD(g).下列判断正确的是( ) A.若温度不变将容器的容积增大1倍.达到新平衡时A的浓度变为原来的0.45倍.则m+n>p+q B.若平衡时.A.B的转化率相等.说明反应开始时.A.B的物质的量之比为m∶n C.若升高平衡体系的温度.达到新平衡时A的浓度变为原来的0.55倍.说明该反应ΔH<0 D.若温度不变.压强增大到原来的2倍.达到新平衡时.总体积一定等于原体积的 解析:将容器的容积增大1倍.A的浓度应变为原来的0.5 倍.现A的浓度变为原来的0.45倍.故减小压强平衡向正反应方向移动.A项错,升高温度.达到新平衡时A的浓度变为原来的0.55倍.故升高温度平衡向正反应方向移动.C项错,增大压强平衡向体积减小的方向移动.达到新平衡时.总体积小于原体积的.若m+n=p+q.D项才能符合题意.D项错. 答案:B
网址:http://m.1010jiajiao.com/timu3_id_79942[举报]
对于平衡体系:mA(g)+nB(g) ![]() pC(g)+qD(g),下列判断正确的是( )
pC(g)+qD(g),下列判断正确的是( )
A.若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.45倍,则m+n>p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
C.若升高平衡体系的温度,达到新平衡时A的浓度变为原来的0.55倍,说明该反应△H<0
D.若温度不变,压强增大到原来的2倍,达到新平衡时,总体积一定比原体积要小
查看习题详情和答案>>对于平衡体系:mA(g)+nB(g) pC(g)+qD(g),下列判断正确的是
pC(g)+qD(g),下列判断正确的是
 pC(g)+qD(g),下列判断正确的是
pC(g)+qD(g),下列判断正确的是[ ]
A.若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.45倍,则m+n>p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C.若升高平衡体系的温度,达到新平衡时A的浓度变为原来的0.55倍,说明该反应ΔH<0
D.压强增大到原来的2倍,达到新平衡时,总体积一定等于原体积的1/2
查看习题详情和答案>>
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C.若升高平衡体系的温度,达到新平衡时A的浓度变为原来的0.55倍,说明该反应ΔH<0
D.压强增大到原来的2倍,达到新平衡时,总体积一定等于原体积的1/2
对于可逆反应,mA(g)+nB (g)  pC(g)+qD (g);H <0有下列判断,其中正确的是
pC(g)+qD (g);H <0有下列判断,其中正确的是
A.若温度不变,将容器的体积扩大1倍,此时A的浓度变为原来的0.6倍,则m+n<q+p
B.若平衡时,A、B的转化率相等,说明反应开始时A、B的物质的量之比为m:n
C.若平衡体系共有气体amol,再向其中加入bmolB,当重新达到平衡时,气体的总物质的量等于(a+b)mol,则m+n>p+q
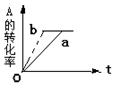
D.加催化剂或增大压强,都能实现如图中a→b的变化

查看习题详情和答案>>