摘要:9. 对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g).下列叙述正确的是( ) A.反应达到平衡时.若两种反应物的转化率相等.则起始投入的n(NH3)∶n(O2)=4∶5 B.反应达到平衡后.对体系一直进行加压.平衡总是向逆向移动 C.反应达到平衡时.若向压强固定的密闭容器中充入稀有气体.平衡不移动 D.当v正(NH3)∶v正(NO)=1∶1时.说明该化学反应已经达到平衡 解析:平衡时.反应物的转化率相等.则起始投入量之比应该等于化学计量数之比.故A正确,当加压到一定压强时.气态水变为非气态水.平衡会向正向移动.故B错,充入稀有气体而压强不变.相当于增大容积.平衡向体积增大的方向移动.C错,NH3.NO的正反应速率都是向右方向的速率.平衡与否其反应速率之比都等于化学计量数之比.故D错. 答案:A
网址:http://m.1010jiajiao.com/timu3_id_79941[举报]
对可逆反应4NH3(g)+5O2(g)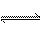 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v逆(H2O)
查看习题详情和答案>>
对可逆反应4NH3(g)+5O2(g)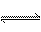 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(CO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看习题详情和答案>>
对可逆反应4NH3(g)+5O2(g)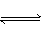 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(CO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看习题详情和答案>>