网址:http://m.1010jiajiao.com/timu3_id_79937[举报]
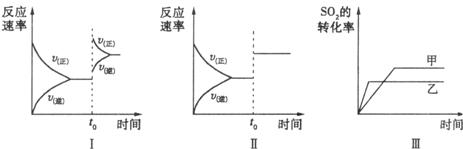
A.图I研究的是t0时刻增大O2的浓度对反应速率的影响
D.图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响
C.图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低
查看习题详情和答案>>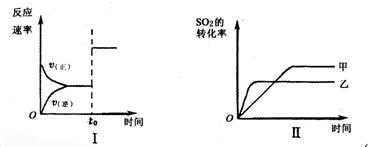
下列叙述正确的是( )
A.图I可以表示t0时刻增大O2的浓度对反应速率的影响
B.图I可以表示t0时刻加入催化剂后对反应速率的影响
C.图Ⅱ可以表示两种不同压强下SO2转化率与时间的关系,且乙的压强比甲高
D.图Ⅱ可以表示两种不同温度下SO2转化率与时间的关系,且甲的温度比乙高
查看习题详情和答案>>小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
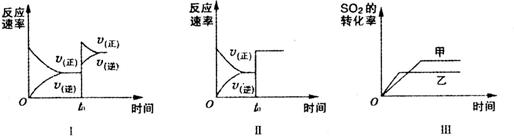
A.图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响
B.图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响
C.图Ⅲ研究的是催化剂对平衡条件的影响,且甲的催化效率比乙高
D.图Ⅲ研究的是温度对化学平衡的影响,且甲的温度较高
查看习题详情和答案>>在容积不变的密闭容器中存在如下反应:
2SO2(g)+O2(g)![]() 2SO3(g);△H=-QkJ/mol(Q>0),
2SO3(g);△H=-QkJ/mol(Q>0),
在其他条件不变时,改变某一条件对上述反应的影响,对下列图象的分析中正确的是

A.图I研究的是t0时刻增大O2的浓度对反应速率的影响
B.图II研究的是t0时刻加入催化剂后对反应速率的影响
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且乙的温度较低
查看习题详情和答案>>在容积不变的密闭容器中存在如下反应: 2SO2(g)+O2(g) 2SO3(g);△H<0,
2SO3(g);△H<0,
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是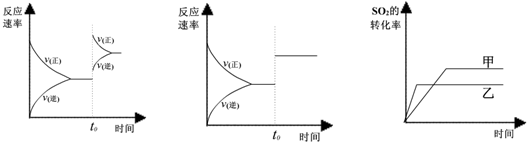
Ⅰ II III
| A.图I研究的是t0时刻增大O2的浓度对反应速率的影响 |
| B.图II研究的是t0时刻加入催化剂后对反应速率的影响 |
| C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D.图III研究的是温度对化学平衡的影响,且乙的温度较低 |