摘要: 在100 mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物.加热充分反应.如图表示加入的混合物的质量与产生的气体体积的关系.试计算: (1)NaOH溶液的物质的量浓度为 . (2)当NaOH溶液的体积为140 mL.固体混合物的质量是51.6 g时.充分反应后.生成气体的体积为 L. (3)当NaOH的溶液的体积为180 mL.固体混合物的质量仍为51.6 g时.充分反应后.生成气体的体积为 L. 解析:(1)从图上看出34.4 g混合物和100 mL NaOH恰好完全反应. n=n(NH3)==0.50 mol.c===5.0 mol·L-1, (2)V=140 mL.因固体过量.所以V(NH3)=22.4 L/mol×n:=22.4 L·mol-1×5 mol·L-1×0.14 L=15.68 L, (3)V=180 mL.过量.固体51.6 g完全反应.=.V(NH3)=16.8 L 答案:(1)5.0 mol·L-1 16.8
网址:http://m.1010jiajiao.com/timu3_id_79076[举报]
在100 mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应,下图表示加入的混合物质量与产生的气体体积(标准状况)的关系,试计算:
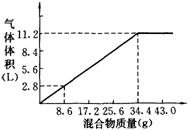
(1)NaOH的物质的量浓度_________;
(2)当NaOH溶液的体积为140 mL,固体混合物的质量是51.6 g时,充分反应后,生成气体的体积(标准状况)为____ L。
(3)当NaOH溶液的体积为180 mL,固体混合物的质量仍为51.6 g时,充分反应后,生成气体的体积(标准状况)为____ L。
查看习题详情和答案>>在100 mL NaOH溶液中加入NH4NO3和 (NH4)2SO4的固体混合物,加热充分反应,如下图表示加入的混合物的质量与产生的气体的体积(标准状况)的关系。
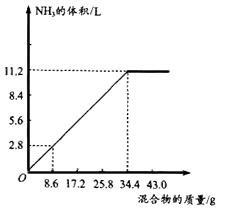
试计算:
(1) NaOH溶液的物质的量浓度;
(2)当NaOH溶液的体积为140 mL,固体混合物的质量是51.6 g时,充分反应后,生成气体的体积(标准状况);
(3)当NaOH溶液的体积为180 mL,固体混合物的质量仍为51.6 g时,充分反应后,生成气体的体积(标准状况)。
查看习题详情和答案>>
(1) NaOH溶液的物质的量浓度;
(2)当NaOH溶液的体积为140 mL,固体混合物的质量是51.6 g时,充分反应后,生成气体的体积(标准状况);
(3)当NaOH溶液的体积为180 mL,固体混合物的质量仍为51.6 g时,充分反应后,生成气体的体积(标准状况)。
在100 mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应,下图表示加入的混合物质量与产生的气体体积(标准状况)的关系,试计算:

(1)NaOH溶液的物质的量浓度为 mol/L。
(2)当NaOH溶液的体积为140mL,固体混合物的质量是51.6g时,充分反应后,生成气
体的体积(标准状况)为 L。
(3)当NaOH溶液的体积为180mL,固体混合物的质量仍为51.6g,充分反应后,生成气体的体积(标准状况)为 L。
查看习题详情和答案>>