摘要:在△ABC中.若│2sinA-1│+(-cosB)=0.则∠C= 0.
网址:http://m.1010jiajiao.com/timu3_id_7904[举报]
 钠是一种非常活泼的金属,露置在空气中会很快与氧气反应生成氧化物,写出该反应的化学方程式
钠是一种非常活泼的金属,露置在空气中会很快与氧气反应生成氧化物,写出该反应的化学方程式4Na+O2=2Na2O
4Na+O2=2Na2O
将其投入水中,它会浮在水面上与水剧烈反应,放出大量热,使自身熔化成小球,甚至使生成的氢气燃烧.其反应的化学方程式为:2Na+2H2O═2NaOH+H2↑,因此钠要保存在煤油中.若在一个烧杯中倒入一定量的水,向水中滴入2滴无色酚酞试液,再加入适量的煤油,然后将一块绿豆大小的钠放入烧杯中,钠会浮在水与煤油的交界处,并与水反应,直至钠消耗完.回答下列问题:反应后水层呈
红
红
色;反应生成的氢气在钠附近不会燃烧,你认为原因是氢气没有与氧气接触
氢气没有与氧气接触
.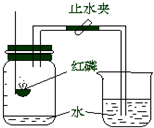 小明想探究空气中氧气的含量,做了如下实验,装置图如图所示.先在集气瓶里加入少量水,再把剩余的容积用记号分成五等分.实验时点燃放在燃烧匙中的红磷,立即塞上橡皮塞.待燃烧完毕冷却后,打开导管上的止水夹.试回答下列问题:
小明想探究空气中氧气的含量,做了如下实验,装置图如图所示.先在集气瓶里加入少量水,再把剩余的容积用记号分成五等分.实验时点燃放在燃烧匙中的红磷,立即塞上橡皮塞.待燃烧完毕冷却后,打开导管上的止水夹.试回答下列问题:(1)等到红磷燃烧完毕,产生的白烟消失后,打开止水夹看到的现象是
有水流入集气瓶中,约占原瓶空气体积的五分之一
有水流入集气瓶中,约占原瓶空气体积的五分之一
.造成这种现象的原因是红磷燃烧消耗了氧气,瓶内气压下降
红磷燃烧消耗了氧气,瓶内气压下降
.(2)由此得出的结论是
空气中氧气约占空气体积的
| 1 |
| 5 |
空气中氧气约占空气体积的
.| 1 |
| 5 |
(3)反思与评价:在实验中,若红磷太少,测得氧气的体积分数会
小于
| 1 |
| 5 |
小于
,若装置的气密性不好,测定氧气的体积分数会| 1 |
| 5 |
小于
| 1 |
| 5 |
小于
.| 1 |
| 5 |
(4)燃烧后,集气瓶中剩余的气体主要是
氮气
氮气
.结合本实验推测该气体的一条化学性质是不支持燃烧等
不支持燃烧等
.(5)在上述实验中,能否用细铁丝来代替红磷进行同样的实验?
不能
不能
原因铁在空气中不能燃烧
铁在空气中不能燃烧
.27、某同学欲用实验室制取氧气(氯酸钾、二氧化锰为原料),完全分解后的残留物来配制一定质量分数的氯化钾溶液,方法是先提纯后配制.
(1)下列实验步骤:A.干燥 B.溶解 C.计算 D.过滤 E.称量 F.蒸发,请按实验顺序填写实验步骤.(写序号)
(2)在实验中,若未将氯化钾干燥就直接配制溶液,则溶液的质量分数将
查看习题详情和答案>>
(1)下列实验步骤:A.干燥 B.溶解 C.计算 D.过滤 E.称量 F.蒸发,请按实验顺序填写实验步骤.(写序号)
BDFACEB
.(2)在实验中,若未将氯化钾干燥就直接配制溶液,则溶液的质量分数将
偏小
.(填偏大、偏小)(2005?海珠区一模)现有一包氯化钠固体,其中混有少量硫酸钠.除去杂质得到纯净氯化钠的实验操作有:
①在溶液中加入稍过量的X溶液,然后过滤
②在滤液中滴加适量的稀盐酸
③蒸发结晶
④将混有杂质的氯化钠完全溶解于水
⑤加入稍过量的BaCl2溶液,然后过滤
请回答:
(1)以上实验操作中,正确合理的操作顺序是(填序号)
(2)在操作①③④中都要用到的同一种仪器是
(3)在操作①中加入的X是(填化学式)
(4)在操作⑤中,若滤液仍浑浊,则应查找原因,并
查看习题详情和答案>>
①在溶液中加入稍过量的X溶液,然后过滤
②在滤液中滴加适量的稀盐酸
③蒸发结晶
④将混有杂质的氯化钠完全溶解于水
⑤加入稍过量的BaCl2溶液,然后过滤
请回答:
(1)以上实验操作中,正确合理的操作顺序是(填序号)
④⑤①②③
④⑤①②③
.(2)在操作①③④中都要用到的同一种仪器是
玻璃棒
玻璃棒
,它在操作④中的作用是加快溶解
加快溶解
.(3)在操作①中加入的X是(填化学式)
Na2CO3(K2CO3)
Na2CO3(K2CO3)
.(4)在操作⑤中,若滤液仍浑浊,则应查找原因,并
重新过滤
重新过滤
.